Медицински експерт на статията
Нови публикации
Синдром на Goodpasture: причини, симптоми, диагноза, лечение
Последно прегледани: 12.07.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
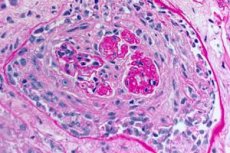
Синдромът на Гудпасчър е автоимунен синдром, включващ алвеоларен белодробен кръвоизлив и гломерулонефрит, причинени от циркулиращи анти-GBM антитела. Синдромът на Гудпасчър най-често се развива при хора с генетична предразположеност, които пушат цигари, но вдишването на въглеводороди и вирусните инфекции на дихателните пътища са възможни допълнителни фактори. Симптомите на синдрома на Гудпасчър включват диспнея, кашлица, умора, хемоптиза и/или хематурия. Синдромът на Гудпасчър се подозира при пациенти с хемоптиза или хематурия и се потвърждава от наличието на анти-GBM антитела в кръвта. Лечението на синдрома на Гудпасчър включва плазмаферинг, глюкокортикоиди и имуносупресори като циклофосфамид. Прогнозата е добра, ако лечението започне преди да се развие дихателна или бъбречна недостатъчност.
Синдромът на Гудпасчър е описан за първи път от Гудпасчър през 1919 г. Синдромът на Гудпасчър е комбинация от гломерулонефрит и алвеоларен кръвоизлив при наличие на анти-GBM антитела. Синдромът на Гудпасчър най-често се проявява като комбинация от дифузен алвеоларен кръвоизлив и гломерулонефрит, но понякога причинява изолиран гломерулонефрит (10-20%) или засягане на белите дробове (10%). Мъжете са засегнати по-често от жените.
Какво причинява синдрома на Гудпасчър?
Причината за заболяването не е точно определена. Предполага се генетична предразположеност към синдрома на Goodpasture, като за негов маркер се счита наличието на HLA-DRW2. Съществува гледна точка за възможната роля на предишна вирусна инфекция (вирус на хепатит А и други вирусни заболявания), производствени опасности и лекарства (предимно D-пенициламин).
В основата на патогенезата на синдрома на Goodpasture е образуването на автоантитела към базалните мембрани на гломерулните капиляри на бъбреците и алвеолите. Тези антитела принадлежат към клас IgG, те се свързват с антителата на базалните мембрани в присъствието на C3 компонента на комплемента с последващо развитие на имунно възпаление на бъбреците и алвеолите на белите дробове.
Анти-GBM антителата са насочени срещу неколагенния (NC-1) домейн на 3-веригата на колаген тип IV, който се намира в най-висока концентрация в базалните мембрани на бъбречните и белодробните капиляри. Излагането на фактори на околната среда - тютюнопушене, вирусни остри респираторни инфекции (ОРИ) и вдишване на хидрокарбонатни суспензии (по-често) - и по-рядко пневмония, активира представянето на алвеоларно-капилярни антигени на циркулиращите антитела при хора с наследствена предразположеност (най-често това са носители на алелите HLA-DRwl5, -DR4 и -DRB1). Циркулиращите анти-GBM антитела се свързват с базалните мембрани, фиксират комплемента и индуцират клетъчен възпалителен отговор, водещ до развитие на гломерулонефрит и/или белодробен капилярит.
Вероятно съществува известна обща черта на автоантигените на базалната мембрана на гломерулните капиляри на бъбреците и алвеолите. Автоантигенът се образува под влияние на увреждащото действие на етиологичния фактор. Неизвестен етиологичен фактор уврежда и модифицира структурата на базалните мембрани на бъбреците и белите дробове. Екскрецията на получените продукти от разграждането на гломерулните базални мембрани на бъбреците се забавя и намалява при тяхното увреждане, което естествено създава предпоставки за развитие на автоимунно увреждане на бъбреците и белите дробове. Все още не е напълно известно кой компонент на базалната мембрана се превръща в автоантиген. Понастоящем се приема, че това е вътрешният структурен компонент на гломерулната базална мембрана на бъбрека, α3-веригата на колаген тип 4.
Образуваните имунни комплекси се отлагат по базалните мембрани на гломерулните капиляри, което води до развитие на имунен възпалителен процес в бъбречния гломерул (гломерулонефрит) и алвеолите (алвеолит). Основните клетки, участващи в развитието на това имунно възпаление, са Т-лимфоцити, моноцити, ендотелиоцити, полиморфонуклеарни левкоцити, алвеоларни макрофаги. Взаимодействието между тях се осигурява от молекулярни медиатори, цитокини (растежни фактори - тромбоцитни, инсулиноподобни, b-трансформиращи; интерлевкин-1, тумор некрозис фактор и др.). Метаболитите на арахидоновата киселина, свободните кислородни радикали, протеолитичните ензими, адхезивните молекули играят основна роля в развитието на имунното възпаление.
Активирането на алвеоларните макрофаги е от голямо значение за развитието на алвеолит при синдрома на Гудпасчър. В активирано състояние те секретират около 40 цитокина. Цитокините от група I (хемотаксини, левкотриени, интерлевкин-8) усилват потока на полиморфонуклеарни левкоцити в белите дробове. Цитокините от група II (растежни фактори - тромбоцити, макрофаги) насърчават движението на фибробластите в белите дробове. Алвеоларните макрофаги също произвеждат активни форми на кислород, протеази, които увреждат белодробната тъкан.
Патоморфология на синдрома на Гудпасчър
Основните патоморфологични прояви на синдрома на Goodpasture са:
- преобладаващо увреждане на микроциркулаторното русло на бъбреците и белите дробове. В белите дробове се наблюдава картина на венулит, артериолит, капиларит с изразени явления на разрушаване и пролиферация; увреждане на капилярите се наблюдава главно в интералвеоларните прегради, развива се алвеолит с хеморагичен ексудат в алвеолите. Увреждането на бъбреците се характеризира с развитие на екстракапиларен пролиферативен гломерулонефрит с последващо образуване на хиалиноза и фиброза, което води до развитие на бъбречна недостатъчност;
- изразени интраалвеоларни кръвоизливи;
- развитие на белодробна хемосидероза и пневмосклероза с различна степен на тежест, в резултат на еволюцията на алвеолит.
Симптоми на синдрома на Гудпасчър
Заболяването най-често се проявява с клинични прояви на белодробна патология. Хемоптизата е най-изразеният симптом; хемоптизата обаче може да отсъства при наличие на хеморагични прояви и пациентът може да се представи само с инфилтративни промени на рентгенография на гръдния кош или с инфилтрат и дихателен дистрес и/или недостатъчност. Диспнея (предимно при усилие), кашлица, неразположение, намалена работоспособност, болка в гърдите, треска и загуба на тегло са чести. До 40% от пациентите имат макрохематурия, въпреки че белодробният кръвоизлив може да предшества бъбречните прояви със седмици до години.
По време на хемоптиза, задухът може да се засили. Слабостта и намалената работоспособност също са проблем.
Симптомите на синдрома на Гудпасчър варират с течение на времето, варирайки от бистри бели дробове при аускултация до пукащи и сухи хрипове. Някои пациенти имат периферни отоци и бледност поради анемия.
По време на прегледа се обръща внимание на бледа кожа, цианоза на лигавиците, пастозност или изразен оток на лицето, намалена мускулна сила и загуба на тегло. Телесната температура обикновено е повишена до фебрилни нива.
При перкусия на белите дробове може да се определи скъсяване на перкусионния звук върху обширни огнища на белодробен кръвоизлив, но това се наблюдава рядко; по-често няма промени в перкусионния звук.
Характерен аускултаторен признак на синдрома на Goodpasture е сухото и влажно хриптене, чийто брой се увеличава значително по време или след хемоптиза.
При изследване на сърдечно-съдовата система се разкрива артериална хипертония, евентуално увеличение на границата на относителната сърдечна тъпота вляво, приглушени сърдечни тонове, мек систоличен шум и шум на перикардно триене се появяват с развитието на тежка бъбречна недостатъчност. При прогресиращо бъбречно увреждане на фона на значителна артериална хипертония може да се развие остра левокамерна недостатъчност с картина на сърдечна астма и белодробен оток. Обикновено тази ситуация се развива в терминалния стадий на заболяването.
Като правило, увреждането на бъбреците се проявява по-късно, след определено време след развитието на белодробни симптоми. Характерни клинични признаци на бъбречна патология са хематурия (понякога макрохематурия), бързо прогресираща бъбречна недостатъчност, олигурия, артериална хипертония.
В 10-15% от случаите синдромът на Goodpasture започва с клинични признаци на бъбречна патология - появява се клиничната картина на гломерулонефрит (олигурия, оток, артериална хипертония, изразена бледност), а след това се присъединяват симптоми на белодробно увреждане. Много пациенти могат да имат миалгия, артралгия.
Независимо от вариантите на начало, синдромът на Goodpasture в повечето случаи протича тежко, заболяването постепенно прогресира, развива се тежка белодробна и бъбречна недостатъчност. Продължителността на живота на пациентите от началото на заболяването варира от няколко месеца до 1-3 години. Най-често пациентите умират от уремия или белодробен кръвоизлив.
Какво те притеснява?
Диагностика на синдрома на Гудпасчър
Диагнозата синдром на Goodpasture изисква откриване на серумни анти-GBM антитела чрез индиректна имунофлуоресценция или, когато е наличен, чрез директен ензимно-свързан имуносорбентен анализ (ELISA) с рекомбинантен човешки NC-1 a3. Други серологични тестове, като например тестване за антинуклеарни антитела (ANA), се използват за откриване на SLE и титър на антистрептолизин-O за откриване на постстрептококов гломерулонефрит, който може да е причина за много случаи на белодробно-бъбречен синдром. ANCA е положителен (в периферни проби) в 25% от случаите на синдром на Goodpasture. Бъбречна биопсия може да бъде показана, ако е налице гломерулонефрит (хематурия, протеинурия, утайка от червени кръвни клетки при анализ на урината и/или бъбречна недостатъчност). Бързо прогресиращ фокален сегментен некротизиращ гломерулонефрит с прогресиращ ход се открива при биопсия при синдром на Goodpasture и всички други причини за белодробно-бъбречен синдром. Имунофлуоресцентното оцветяване на бъбречната или белодробната тъкан класически разкрива линейно отлагане на IgG по гломерулните или алвеоларните капиляри. Наблюдава се също при диабетен бъбречен и фибриларен гломерулонефрит, рядко заболяване, причиняващо белодробно-бъбречен синдром, но откриването на GBM антитела при тези заболявания е неспецифично.
Тестовете за белодробна функция и бронхоалвеоларният лаваж не са диагностични за синдрома на Goodpasture, но могат да се използват за потвърждаване на наличието на дифузен алвеоларен кръвоизлив при пациенти с гломерулонефрит и белодробни инфилтрати, но без хемоптиза. Лаважната течност, която остава хеморагична след многократни промивки, може да потвърди дифузен хеморагичен синдром, особено ако има съпътстващо понижение на хематокрита.
 [ 3 ]
[ 3 ]
Лабораторна диагностика на синдрома на Гудпасчър
- Общ кръвен анализ. Характерни белези са желязодефицитна хипохромна анемия, хипохромия, анизоцитоза, пойкилоцитоза на еритроцитите. Наблюдават се също левкоцитоза, изместване на левкоцитната формула наляво и значително повишаване на СУЕ.
- Общ анализ на урината. В урината се откриват протеин (степента на протеинурия може да бъде значителна), цилиндри (гранулирани, хиалинови, еритроцитни), еритроцити (може да се появи макрохематурия). С прогресирането на хроничната бъбречна недостатъчност относителната плътност на урината намалява и при теста на Зимницки се развива изохипостенурия.
- Биохимичен кръвен тест. Повишени нива на урея, креатинин, хаптоглобин, серомукоид, а2 и гама глобулини в кръвта, намалено съдържание на желязо.
- Имунологични изследвания. Може да се открие намаляване на броя на Т-лимфоцитните супресори, откриват се циркулиращи имунни комплекси. Антитела към базалната мембрана на гломерулните и алвеоларните капиляри се откриват чрез индиректна имунофлуоресценция или радиоимунологични методи.
- Анализ на храчки. Храчките съдържат много еритроцити, хемосидерин, откриват се сидерофаги.
Инструментална диагностика на синдрома на Goodpasture
- Рентгеново изследване на белите дробове. Характерни рентгенови признаци са белодробни инфилтрати в кореновата област, разпространяващи се към долните и средните части на белите дробове, както и прогресивни, симетрични, двустранни облакоподобни инфилтрати.
- Изследване на функцията на външното дишане. Спирометрията разкрива рестриктивен тип дихателна недостатъчност (намален жизнен капацитет), с напредването на заболяването се присъединява обструктивен тип дихателна недостатъчност (намален FEV1, индекс на Тифено).
- ЕКГ. Разкриват се признаци на тежка миокардна дистрофия с анемичен и хипоксичен генезис (намаляване на амплитудата на Т-вълните и ST интервала в много отвеждания, най-често в левите гръдни отвеждания). При тежка артериална хипертония се появяват признаци на левокамерна миокардна хипертрофия.
- Анализът на кръвните газове разкрива артериална хипоксемия.
- Изследване на белодробни и бъбречни биопсии. Биопсия на белодробната тъкан (отворена биопсия) и бъбреците се извършва за окончателно потвърждаване на диагнозата, ако е невъзможно точното диагностициране на заболяването с помощта на неинвазивни методи. Извършва се хистологично и имунологично изследване на биопсиите. Следните признаци са характерни за синдрома на Goodpasture:
- наличието на морфологични признаци на гломерулонефрит (най-често екстракапиларен), хеморагичен алвеолит, хемосидероза и интерстициална фиброза;
- откриване на линейни отлагания на IgG и комплементен компонент C3 върху базалните мембрани на белодробните алвеоли и бъбречните гломерули, използвайки имунофлуоресцентния метод.
Диагностични критерии за синдром на Гудпасчър
При поставяне на диагноза синдром на Goodpasture е препоръчително да се използват следните критерии.
- Комбинация от белодробна патология и бъбречна патология, т.е. хемоптиза (често белодробен кръвоизлив), задух и симптоми на гломерулонефрит.
- Постоянно прогресиращ ход на заболяването с развитие на дихателна и бъбречна недостатъчност.
- Развитие на желязодефицитна анемия.
- Откриване по време на рентгенографско изследване на белите дробове на множество двустранни облачноподобни инфилтрати на фона на ретикуларна деформация на белодробния модел.
- Откриване в кръвта на високи титри на циркулиращи антитела към базалната мембрана на бъбречните гломерули и алвеоли.
- Откриване на линейни отлагания на IgG и комплементен компонент C3 върху базалните мембрани на гломерулните и алвеоларните капиляри.
- Липса на други системни (с изключение на белодробни и бъбречни) прояви.
Диференциална диагноза на синдрома на Гудпасчър
Синдромът на Гудпасчър трябва да се диференцира от редица заболявания, проявяващи се с хемоптиза или белодробен кръвоизлив. Необходимо е да се изключат онкологични заболявания на бронхите и белите дробове, туберкулоза, белодробни абсцеси, бронхиектазии, сърдечно-съдови заболявания (водещи до застой и хипертония в белодробното кръвообращение), системен васкулит, хеморагична диатеза.
Програма за скрининг на синдрома на Гудпасчър
- Общи изследвания на кръв и урина.
- Биохимичен кръвен тест: определяне на общ протеин и протеинови фракции, креатинин и урея, трансаминази, серомукоид, хаптоглобин, фибрин, желязо.
- Анализ на храчки: цитологично изследване, определяне на сидерофаги.
- Имунологични изследвания: определяне на съдържанието на В- и Т-лимфоцити, субпопулации от Т-лимфоцити, имуноглобулини, циркулиращи имунни комплекси, антитела към базалните мембрани на гломерулите на бъбреците и алвеолите.
- Рентгеново изследване на белите дробове.
- ЕКГ.
- Спирометрия.
- Изследване на биопсии от бели дробове и бъбреци.
Какво трябва да проучим?
Какви тестове са необходими?
Лечение на синдрома на Гудпасчър
Лечението на синдрома на Goodpasture включва ежедневен или през ден плазмаферез в продължение на 2 до 3 седмици (4 L плазмаферез) за отстраняване на анти-GBM антитела, комбиниран с интравенозни глюкокортикоиди (обикновено метилпреднизолон 1 g в продължение на поне 20 минути през ден 3 пъти с преднизолон 1 mg/kg телесно тегло дневно) и циклофосфамид (2 mg/kg веднъж дневно) в продължение на 6 до 12 месеца, за да се предотврати образуването на нови антитела. Терапията може да бъде намалена постепенно, когато белодробната и бъбречната функция престанат да се подобряват. Дългосрочната смъртност е свързана със степента на бъбречно увреждане в началото на заболяването; пациентите, нуждаещи се от диализа рано, и тези с повече от 50% полумесести нефрони при биопсия, имат време на преживяемост по-малко от 2 години и често се нуждаят от диализа, освен ако не се обмисля бъбречна трансплантация. Хемоптизата може да бъде добър прогностичен признак, тъй като води до по-ранно откриване на заболяването; малцинството от пациентите, които са ANCA-позитивни, реагират по-добре на лечение за синдром на Goodpasture. Рецидив се наблюдава в малък процент от случаите и е свързан с продължаващо тютюнопушене и инфекция на дихателните пътища. При пациенти с терминална бъбречна недостатъчност, на които е извършена бъбречна трансплантация, заболяването може да рецидивира в присадката.
Каква е прогнозата за синдрома на Гудпасчър?
Синдромът на Гудпасчър често е бързо прогресиращ и може да бъде фатален, освен ако не бъде диагностициран и лекуван своевременно; прогнозата е добра, когато лечението започне преди да се развие дихателна или бъбречна недостатъчност.
Незабавното оцеляване по време на белодробен кръвоизлив и дихателна недостатъчност е свързано с осигуряване на проходимост на дихателните пътища; ендотрахеална интубация и механична вентилация се препоръчват при пациенти с гранични нива на газове в артериалната кръв и предстояща дихателна недостатъчност.

