Медицински експерт на статията
Нови публикации
Криптококов менингит
Последно прегледани: 23.11.2021

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
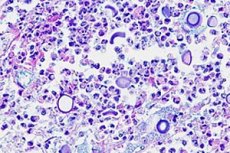
Възпалението на меките мембрани на мозъка може да бъде причинено не само от бактерии, вируси и протисти, но и от гъбична инфекция. Криптококов менингит се развива, когато е засегната капсулираната мая Cryptococcus neoformans, която принадлежи към човешки условно патогенни патогени. [1] Наречена е болест на Busse-Buschke поради първото си описание от Ото Бусе и Ейбрахам Бушке през 1894 г. [2]
Според МКБ-10 кодът на заболяването е G02.1 (в раздела за възпалителни заболявания на централната нервна система), както и B45.1 в раздела за микози (тоест гъбични заболявания).
Епидемиология
Осем от десет случая на криптококов менингит засягат хора с ХИВ / СПИН.
Според данните, публикувани от The Lancet Infe заразни болести през пролетта на 2017 г., сред хората с ХИВ или СПИН тази гъба причинява около 220 хиляди случая на криптококов менингит годишно, а повече от 180 хиляди души умират. Повечето случаи на криптококов менингит се срещат в Африка на юг от Сахара.
Според статистиката на СЗО, през 2017 г. Са регистрирани 165,8 хиляди случая на криптококов менингит в Африка, 43,2 хиляди в Азия, 9,7 хиляди в Северна и Южна Америка и 4,4 в европейските страни. Хиляди случаи на болестта.
Причини криптококов менингит
Причините за този вид менингит са инфекция с гъбата Cryptococcus neoformans (клас Tremellomycetes, род Filobasidiella), която живее в околната среда: в почвата (включително прах), върху гниеща дървесина, в изпражненията на птици (гълъби) и прилепи и т.н.... Заразяването става по аерогенен път - чрез вдишване на аерозолни базидиоспори на гъбата, въпреки че при повечето хора с достатъчно ниво на имунитет, C. Neoformans не води до развитие на болестта и остава незадължителен вътреклетъчен опортюнистичен микроорганизъм (който не може да зарази други хора ). Прочетете също - Криптококи - причинителите на криптококозата [3]
По правило криптококовият менингит се развива при HIV -инфектирани (стадий IVB) - като вторична инфекция, както и при хора с лошо функционираща имунна система при други заболявания, придружени от продължителна имуносупресия. [4]
Възпалението на менингите, дължащо се на криптококи, се счита за церебрална или извънбелодробна форма на криптококоза , която възниква след хематогенно разпространение на C. Neoformans от дихателните пътища и белите дробове до мозъка и гръбначния мозък. [5]
Рискови фактори
Факторите с най -голям риск от развитие на криптококов менингит са:
- неонатален период (неонатален период) и недоносени бебета;
- отслабване на имунната система при рак (включително левкемия, множествен меланом, лимфосаркома), при пациенти с HIV инфекция и СПИН ;
- диабет;
- вирусен хепатит и други имунокомплексни заболявания;
- сърповидно-клетъчна анемия;
- химиотерапия при наличие на онкологична диагноза;
- превишаване на допустимата норма на йонизиращо лъчение;
- дълги курсове на лечение с антибиотици или стероиди;
- инсталиране на вътресъдови катетри и шунтове;
- трансплантация на костен мозък или вътрешни органи.
Патогенеза
Криптококите, защитени от човешки имунни клетки чрез полизахаридна капсула (потискаща фагоцитозата), секретират протеази, уреаза, фосфолипаза и нуклеаза, ензими, които могат да унищожат клетките гостоприемници. [6]
И патогенезата на криптококозата се крие във факта, че тези ензими увреждат клетките чрез лизис на мембрани, модификация на молекули, дисфункция на клетъчните органели и промени в цитоскелета. [7]
Гъбичните серинови протеази разрушават пептидните връзки на клетъчните протеини, разграждат имуноглобулините и протеините на имунните ефекторни клетки, а C. Neoformans се репликира вътре в мононуклеарните фагоцити (макрофаги), което улеснява тяхната пролиферация. [8]
Освен това, преминавайки през ендотелни клетки и чрез трансфер вътре в заразените макрофаги, криптококите нарушават целостта на кръвно-мозъчната бариера (BBB). Гъбата се разпространява през кръвния поток в цереброспиналната течност и след това в меките мембрани на мозъка с образуването на „колонии“ от гъбични клетки в мозъчните тъкани под формата на желатинови псевдокисти. [9]
Симптоми криптококов менингит
Първите признаци на криптококов менингит са треска (повишаване на температурата до + 38,5-39 ° C) и силно главоболие.
Също така клиничните симптоми се проявяват с гадене и повръщане, гърчове, скованост (скованост) на шията, повишена чувствителност на очите към светлина, нарушено съзнание и поведение. [10]
Според експерти развитието на менингиалния синдром е по -бавно, отколкото при бактериално увреждане на менингите.
Усложнения и последствия
Усложненията и последиците от гъбичния менингит, причинени от криптокок са:
- значително повишаване на вътречерепното налягане;
- изолирано увреждане на черепните нерви с пареза / парализа на лицето и атрофични промени в зрителния нерв (водещи до офталмологични проблеми);
- разпространението на възпалителния процес в тъканта на подкортекса и мозъчните полукълба - криптококов менингоенцефалит;
- развитие на мозъчен абсцес (криптококома);
- излив в субдуралното пространство (под твърдата мозъчна обвивка);
- нараняване на гръбначния мозък;
- умствени промени и намалени когнитивни функции.
Диагностика криптококов менингит
В допълнение към анамнезата и медицинския преглед, диагнозата на инфекция с C. Neoformans при менингит задължително включва кръвни изследвания: общи клинични и биохимични, анализ на кръвния серум за антитела към протеините на C. Neoformans, кръвна култура.
Извършва се лумбална пункция и се прави анализ на цереброспиналната течност за антиген и бактериоскопски анализ (бактериална култура) на цереброспиналната течност. [11]
Инструменталната диагностика се извършва с помощта на рентгенова снимка на гръдния кош и магнитен резонанс на мозъка.
Диференциална диагноза
Диференциалната диагноза включва менингит и менингоенцефалит с бактериална и вирусна етиология, мозъчно увреждане от Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis или амеби (включително Naegleria fowleri).
Лечение криптококов менингит
Етиологичното лечение е насочено към изкореняване на криптококи, за които се използват противогъбични лекарства.
Режимът на лечение включва интравенозно приложение (капково, през централен венозен катетър или чрез перитонеална инфузия) на полиен противогъбичен антибиотик Амфотерицин В (Амфоцил) в комбинация с противогъбично средство Флуцитозин (5-флуороцитозин) или Флуконон, който има фунгициден и фунгистатичен ефект. Дозировката на тези лекарства се изчислява в зависимост от телесното тегло на пациента.
Необходимо е постоянно наблюдение на състоянието на пациента, тъй като амфотерицин В има токсичен ефект върху бъбреците, а страничните ефекти на флуцитозин могат да бъдат инхибиране на хемопоетичната функция на костния мозък, спиране на дишането или сърцето, развитие на кожни лезии под формата на епидермална некролиза и др.
Според препоръките, публикувани в актуализацията на IDSA за 2010 г. (Американското дружество по инфекциозни болести), лечението не се е променило от десет години. Противогъбичното лечение от първа линия се основава на индуциране, консолидиране и поддържане на следните три типа пациенти: [12]
Болести, свързани с ХИВ
- Индукционна терапия
- Амфотерицин В дезоксихолат (0,7-1,0 mg / kg / ден) + флуцитозин (100 mg / kg / ден перорално) за 2 седмици (доказателство А1)
- Липозомален амфотерицин В (3-4 mg / kg / ден) или амфотерицин В липиден комплекс (5 mg / kg / ден; мониторинг на бъбречната функция) + флуцитозин (100 mg / kg / ден) за 2 седмици (доказателство В2)
- Амфотерицин В дезоксихолат (0,7 до 1,0 mg / kg / ден) или липозомален амфотерицин В (3 до 4 mg / kg / ден) или липиден комплекс амфотерицин В (5 mg / kg / ден, за пациенти с непоносимост към флуцитозин) за 4 до 6 седмици (доказателство В2)
- Алтернативи на индукционната терапия
- Амфотерицин В дезоксихолат + флуконазол (доказателства В1)
- Флуконазол + флуцитозин (доказателство В2)
- Флуконазол (доказателства за В2)
- Итраконазол (доказателство за С2)
- Флуконазол (400 mg / ден) за 8 седмици (данни А1)
- Флуконазол (200 mg / ден) за 1 или повече години (доказателство А1)
- Итраконазол (400 mg / ден) за 1 или повече години (доказателство C1)
- Амфотерицин В дезоксихолат (1 mg / kg / седмица) за 1 или повече години (доказателство C1)
- Консолидираща терапия
- Поддържаща терапия
- Алтернативи на поддържаща грижа
Болести, свързани с трансплантацията
- Индукционна терапия
- Липозомен амфотерицин В (3-4 mg / kg / ден) или липиден комплекс амфотерицин В (5 mg / kg / ден) + флуцитозин (100 mg / kg / ден) за 2 седмици (доказателство В3)
- Алтернативи на индукционната терапия
- Липозомен амфотерицин В (6 mg / kg / ден) или липиден комплекс амфотерицин В (5 mg / kg / ден) за 4-6 седмици (доказателство В3)
- Амфотерицин В дезоксихолат (0,7 mg / kg / ден) за 4-6 седмици (доказателство В3)
- Флуконазол (400 до 800 mg / ден) за 8 седмици (доказателство В3)
- Флуконазол (200 до 400 mg / ден) от 6 месеца до 1 година (доказателство В3)
- Консолидираща терапия
- Поддържаща терапия
Болест, не свързана с ХИВ / трансплантация
- Индукционна терапия
- Амфотерицин В дезоксихолат (0,7 до 1,0 mg / kg / ден) + флуцитозин (100 mg / kg / ден) за 4 седмици или повече (доказателство В2)
- Амфотерицин В дезоксихолат (0,7-1,0 mg / kg / ден) за 6 седмици (доказателство В2)
- Липозомен амфотерицин В (3-4 mg / kg / ден) или липиден комплекс амфотерицин В (5 mg / kg / ден) плюс флуцитозин, 4 седмици (доказателство В3)
- Амфотерицин В дезоксихолат (0,7 mg / kg / ден) + флуцитозин (100 mg / kg / ден) за 2 седмици (доказателство В2)
- Консолидираща терапия
- Флуконазол (400 до 800 mg / ден) за 8 седмици (доказателство В3)
- Флуконазол (200 mg / ден) за 6-12 месеца (доказателство В3)
- Поддържаща терапия
Комбинацията от амфотерицин В и флуцитозин е най -ефективната мярка за елиминиране на инфекцията и показва по -голяма полза за преживяемост в сравнение само с амфотерицин. Въпреки това, поради своята цена, флуцитозин често не е наличен в условия с ограничен ресурс, където тежестта на заболяването е значителна. Комбинация на амфотерицин В и флуконазол са изследвани и са получени най-добри резултати в сравнение с един с амфотерицин В. [13], [14], [15]
Без лечение клиничният ход преминава в объркване, припадъци, понижено ниво на съзнание и кома.
Болкоустойчивото главоболие може да се лекува с гръбначна декомпресия след адекватна оценка на невроизображението с компютърна томография или ЯМР. Безопасният максимален обем цереброспинална течност, който може да се източи в една лумбална пункция, е неясен, но често до 30 ml се отстраняват с проверка на налягането след отстраняване на всеки 10 ml. [16]
Предотвратяване
Предотвратяването на инфекция от гъбичките Cryptococcus neoformans е необходимо преди всичко със слаба имунна система. [17]Препоръчва се да се избягват прашни зони и да се работи със земя, а ХИВ-позитивните хора трябва да получават постоянна антиретровирусна терапия.
Прогноза
Без лечение прогнозата за всеки гъбичен менингит е лоша.
Първоначалната прогноза зависи от предиктори за смъртността, като например следното [18], [19]:
- Налягането при отваряне на цереброспиналната течност е повече от 25 cm вода. Изкуство.
- Нисък брой на белите кръвни клетки в цереброспиналната течност
- Сензорно увреждане
- Късна диагноза
- Повишени титри на антигени на CSF
- Степен на изчистване на инфекцията
- Количеството мая в CSF надвишава 10 mm 3 (обичайна практика в Бразилия) [20]
- Пациенти без ХИВ и прогностични фактори при тези пациенти, в допълнение към вече споменатите:
- Маркери на слаб възпалителен отговор
- Без главоболие
- Основно хематологично злокачествено новообразувание
- Хронично бъбречно или чернодробно заболяване
Смъртността варира в различните страни в зависимост от настройките на ресурса. Той остава висок в САЩ и Франция, като 10-седмичната смъртност варира от 15% до 26% и дори по-висока при пациенти без ХИВ поради късна диагноза и дисфункционални имунни отговори. От друга страна, в условия с ограничен ресурс, смъртността се увеличава от 30% на 70% за 10 седмици поради късен достъп до грижи и липса на достъп до лекарства, манометри и оптимално наблюдение.

