Медицински експерт на статията
Нови публикации
Инструментална и лабораторна диагностика на рака на ректума
Последно прегледани: 04.07.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
Съвременната медицина разполага с голям брой методи за прецизна диагностика на злокачествени заболявания на червата. Такива методи включват както инструментални, така и неинструментални изследвания, рентгенография, физиологични и бактериологични изследвания и др.
Диагнозата на рак на ректума обикновено се счита за цялостен преглед. На първия етап от пациента се взема кръв за клиничен и биохимичен анализ, след което се изследват изпражненията.
Дигиталният ректален преглед също е задължителен от много години – често именно с тази процедура започва стандартната диагностична схема. Какво може да даде на лекаря този или онзи вид преглед? Нека разгледаме този въпрос по-подробно.
Начален етап на диагностициране на рак на ректума
Ако се подозира раков тумор, по време на прегледа понякога се откриват признаци като уголемяване на корема, външни фистулни изходи и уголемени лимфни възли. Перкусия на корема може да открие натрупване на течност (асцит) или газове по време на чревна перфорация.
Палпацията на корема, въпреки привидната си простота, се счита за много ценна процедура за определяне на туморния процес. Благодарение на палпацията е възможно да се оцени степента на мускулно напрежение, наличието на спазми и течности и др. Лекарят задължително изследва всички лимфни възли, които могат да бъдат засегнати от патологичния процес.
Прегледът на перинеалната област ни позволява да видим промени в кожата и аналния сфинктер, което също може да бъде ценна информация за диагнозата.
Дигиталният ректален преглед се счита за проста, но много информативна процедура. Той се извършва както по време на превантивно посещение при лекар, така и при наличие на оплаквания, свързани с работата на долните черва. Ако такъв преглед се проведе внимателно и компетентно, тогава е напълно възможно да се оцени състоянието на по-голямата част от ректума и дори да се постави предварителна диагноза. Как се извършва процедурата: лекарят вкарва пръст в ректума и опипва стените му отвътре. Прегледът може да не е много приятен, но е безболезнен.
Тестове за предполагаем рак на ректума
Какви лабораторни изследвания обикновено се предписват при съмнение за рак?
- Фекалии за скрита кръв - този метод определя дали има скрито кървене или кървене на тумора. За да бъде резултатът възможно най-точен, фекалиите трябва да се подават няколко пъти, а за профилактика - веднъж годишно.
- Пълна кръвна картина – помага да се определи дали човек има анемия, свързана със скрита загуба на кръв. Ниските нива на хемоглобина могат да бъдат един от първите показатели за рак.
- Биохимичното изследване на кръвта е оценка на карциноембрионалния антиген (CEA), чието ниво определя стадия на злокачествения процес. Биохимичното изследване обикновено се предписва преди и след операцията. Като правило, в рамките на 2 месеца след радикална операция, съдържанието на CEA се връща към нормалното. При наличие на метастази или развитие на рецидив на онкопатологията, стойностите му отново се повишават.
- ДНК тестът във фекалиите е специфичен анализ, който се извършва за откриване на мутирали гени, т.е. променени клетъчни структури, които водят до развитие на злокачествена патология.
 [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
Туморни маркери за рак на ректума
Както е известно, трудността при диагностицирането на раков тумор до голяма степен се обяснява с неговия асимптоматичен ход, когато пациентът търси помощ само когато болестта е отишла твърде далеч. Поради тази причина учените отдавна търсят диагностичен метод, който би помогнал за възможно най-ранното идентифициране на патологията. И този метод беше намерен - това е определението за туморни маркери.
Какво представляват те? Туморните маркери са уникални протеинови вещества, отделяни по време на жизнената активност на туморните клетки. Те се определят в кръвта или урината на пациент с онкология. В същото време, с помощта на съвременни средства, е възможно да се определи повишаване на нивото на такива вещества дори в ранните стадии на рака.
Какво показва нивото на маркера:
- в кой орган може да се намира неоплазмата;
- ефективно ли беше предписаното лечение;
- възможно ли е патологията да се развие отново;
- има ли риск от развитие на рак в бъдеще.
Съществуват редица туморни маркери, които показват наличието и локализацията на раковия процес в ректума. Това са маркери като AFP, CA 72-4, LASA-P, CA 242, CA 19-9, CYFRA 21-1.
Въпреки това, има и някои недостатъци на маркерния анализ:
- туморните маркери не са строго специфични - например, един и същ индикатор може да показва наличието на процес във всяка част на храносмилателната система;
- високите нива на маркери не винаги могат да се интерпретират като наличие на тумор;
- При някои здрави хора също може да се открият тези вещества.
От всичко гореизложено могат да се направят следните заключения: определянето на маркери е важна процедура, но диагноза не може да се постави само въз основа на тяхното повишаване. Диагностиката трябва да се приема цялостно, като се използват всички възможни методи.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Инструментална диагностика на рак на ректума
Целта на инструменталната диагностика на ректума е да се визуализира увредената от патологията област, да се определи естеството на лезията и нейния стадий, да се вземе тъканна проба за по-подробно изследване (биопсия), както и предварителна оценка на метастазите.
- Аноскопията е метод за изследване на ректума с помощта на аноскоп, инструмент, който се вкарва през аналния сфинктер и позволява да се изследва вътрешната повърхност на лигавицата. Дълбочината на възможното изследване е около 15 см.
- Ректоманоскопията се извършва с помощта на ректоскоп, който се вкарва в ректума и на разстояние до 50 см. Тази техника позволява на лекаря да изследва лигавиците на червата, с възможност за вземане на тъканни проби за допълнителен анализ. Процедурата не може да се нарече приятна или напълно безболезнена, но като диагностика тя често е просто незаменима.
- Фиброколоноскопията ви позволява да изследвате вътрешната повърхност на червата, да определите точно местоположението на тумора, да вземете парченца материал за биопсия и дори да премахнете малки полипи. С този метод можете да оцените състоянието на дебелото черво по цялата му дължина.
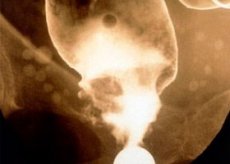
- Иригоскопията включва въвеждането на специално контрастно вещество в чревната кухина чрез клизма, което ще засенчи вътрешната кухина на червата при изследването им на рентгенови снимки. Тази процедура се използва главно при пациенти в напреднала възраст, а също и ако лекарят подозира няколко туморни процеса в червата едновременно.
- Интравенозна урография може да бъде предписана като допълнителен метод за изследване, например, ако тумор е нараснал в пикочния мехур.
- Ултразвуковото наблюдение на коремните органи се използва за откриване на метастази. Ако процедурата се извършва с натрупване на течност (асцит), тогава ултразвукът ви позволява да оцените нейния обем.
- Методът на компютърна томография се използва за определяне на растежа на тумора в близките органи, откриване на метастази и проверка на най-близките лимфни възли.
- Диагностичната лапароскопия е минимално инвазивна хирургична процедура, при която коремната стена се пробива на няколко места и през пробивите се вкарва специална камера, която позволява не само да се види наличието на метастази в коремната кухина, но и да се отстранят малки обекти.
Бих искал да се спра отделно на метода на магнитно-резонансната томография, който, макар и да не се счита за приоритетно изследване, понякога може да предостави много важна информация на лекаря. Определяне на степента на растеж на тумора, избор на терапевтичен режим, оценка на необходимостта и обхвата на операцията - това са точно случаите, когато тази процедура е просто необходима. Освен това, ЯМР позволява да се наблюдава и оценява ходът на лечението на рака и да се определят по-нататъшни тактики по отношение на пациента.
Ракът на ректума на ЯМР ще бъде по-добре визуализиран и оценен от лекаря, ако следвате тези препоръки:
- Преди процедурата трябва да почистите ректума - това може да се направи с слабително или обикновена почистваща клизма;
- 1-1,5 часа преди процедурата трябва да изпразните пикочния си мехур, след което пиенето не е разрешено до края на прегледа;
- Препоръчва се прием на 3 таблетки дротаверин (Но-шпа) приблизително един час преди ЯМР.
Ако всичко е направено правилно, лекарят ще може лесно да извърши следните действия:
- вижте самия тумор, включително неговите граници;
- определят връзката на неоплазмата с тазовите органи и сфинктера;
- определят състоянието на тазовите мускули;
- оценка на състоянието на лимфната система в таза;
- да се следи ефективността на операцията, химиотерапията или лъчетерапията и да се проследява заболяването във времето.
Хистологични и цитологични изследвания
За да се разграничи доброкачествено заболяване от злокачествено, се използва изследване като биопсия, последвано от хистологичен анализ. Благодарение на биопсията е възможно с голяма точност да се установи наличието или отсъствието на раков тумор в изследваните тъкани. Диагностичният метод включва отстраняване на малък елемент от туморната тъкан - целият процес се извършва по време на ректоскопия и не причинява допълнителен дискомфорт на пациента. Полученото парче тъкан се подлага на хистологична и цитологична оценка.
В допълнение към ректоскопията, лекарят може да вземе необходимия материал по време на лапароскопия, операция или фиброколоноскопия. •
Хистологичното изследване включва изследване на проба от отстранена тъкан с помощта на микроскопски метод и може да се извърши по спешност или по план:
- спешна хистология се извършва за около половин час, когато е необходим бърз резултат. Пробата първо се замразява, след което се третира със специфични багрила и се изследва с помощта на микроскоп;
- Планираната хистология обикновено трае поне 5 дни. Получената проба се покрива със специална течност и парафин и се боядисва. Този метод на изследване се счита за по-сложен в сравнение със спешната хистология. Резултатите от нея обаче са по-точни и надеждни.
Като правило, за да се гарантира, че резултатите от хистологичното изследване няма да бъдат поставени под въпрос в бъдеще, то се извършва от поне двама специалисти. •
Цитологичното изследване е оценка на клетъчните структури на тъканите, която позволява да се забележат злокачествени промени в тях. По какво се различава този анализ от хистологичния? По това, че цитологичният метод включва изследване не на тъканен срез, а на отделни туморни клетки.
Следният биологичен материал може да се използва за извършване на цитология:
- тъканни проби, взети по време на биопсия от необходимата част на червата;
- гнойно или слузесто отделяне от чревната кухина;
- проби от отпечатъци от лигавична тъкан от съответния участък на червата.
Само горепосочените методи ни позволяват да определим със сигурност кой тумор трябва да се лекува: доброкачествен или злокачествен.
Диференциална диагноза на рак на ректума
Ракът на ректума трябва да се разграничава от следните заболявания:
- доброкачествени полипи;
- хроничен улцерозен проктосигмоидит с дизентериен, амебен и туберкулозен произход;
- колит, ректален пролапс, неспецифичен гранулом;
- сифилис, актиномикоза;
- меланобластоми на аналния ректум;
- растеж на тумор от матката, влагалището, простатата;
- злокачествен карциноид;
- хемороиди и фисури на аналния сфинктер.
За да се разграничи раков тумор в ректума от полипи, се предписва ендоскопско изследване - колоноскопия. Този метод позволява да се видят в лумена на червата не само големи полипи, но и язви на лигавицата, възпалителни елементи, малки сплескани полипи, деформирани съдове и др. Същият метод може да се използва за разграничаване на рак от проктосигмоидит - възпалителен процес в сигмоидеята и ректума.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ]
Как да различим хемороидите от рак на ректума?
Понякога определени признаци играят решаваща роля, чрез които човек може да различи туморния процес от обикновените хемороиди.
- Ако пациентът преди това е бил диагностициран с полипи, съществува риск те да се дегенерират в раков тумор.
- Хемороидалната кръв се отделя в края на акта на дефекация, под формата на ивици и петна върху изпражненията. В случай на рак, кръвта не е на повърхността, а е смесена с изпражненията.
- В случай на тумор, преди дефекация може да има слузесто отделяне, понякога с гной и парченца тъкан.
- При обширен тумор изпражненията са подобни на лента, а трудната дефекация може да продължи дълго време, до няколко дни.
- Туморният процес е съпроводен с измършавяване на пациентите, слабост и летаргия.
- При наличие на метастази, функционирането на други органи започва да се влошава.
Въпреки това, във всеки случай, за да се установи точна диагноза, е необходимо да се проведе биопсия с хистологично изследване на тъканите. Едва след това може уверено да се заяви наличието или отсъствието на злокачествен процес.
Диагностиката на рак на ректума трябва да се извършва при най-малкото съмнение за неговото наличие. Много е важно злокачественото заболяване да се открие възможно най-рано - това ще позволи навременно лечение, което значително ще подобри прогнозата и ще ускори възстановяването.

