Нови публикации
Медикаменти
Невролептици или антипсихотици
Last reviewed: 24.06.2018

Имаме строги насоки за източници и свързваме само с реномирани медицински сайтове, академични изследователски институции и, когато е възможно, с медицински рецензирани изследвания. Обърнете внимание, че числата в скоби ([1], [2] и т.н.) са връзки към тези изследвания, върху които може да се кликва.
Ако смятате, че някое от нашите съдържания е неточно, остаряло или по друг начин съмнително, моля, изберете го и натиснете Ctrl + Enter.
Антипсихотиците (невролептиците) са клас психотропни лекарства, използвани предимно за лечение на шизофрения. Понастоящем е общоприето да се разграничават две групи (или категории) лекарства: типични и атипични антипсихотици. По-долу е дадена информация за фармакологичните свойства, показанията за употреба и страничните ефекти на терапията за всяка от тези групи лекарства.
Показания за употреба на типични антипсихотици
В момента основните показания за предписване на традиционни невролептици, според препоръките, предоставени от авторитетни изследователи в областта на психофармакотерапията, включват следното.
- Облекчаване на психомоторна възбуда и поведенчески разстройства, причинени от тежки психотични симптоми. В тези случаи е показано използването на перорални или парентерални форми на лекарства с антипсихотично действие, както глобално (клопромазин, левомепромазин, тиопроперазин, цуклопентиксол), така и селективно - под формата на ефект върху халюцинаторно-параноидни разстройства (халоперидол, трифлуоперазин).
- Антирецидивна (превантивна) терапия. За тази цел се предписват депо форми на лекарства, особено при пациенти с лошо спазване на лекарствената терапия (халоперидол деканоат, удължена форма на флупентиксол), или малки или средни дози лекарства за получаване на дезинхибиторен (антинегативен) ефект, измежду тези лекарства, чиито високи дози се използват за облекчаване на остри психотични разстройства (флупентиксол, зуклопентиксол). При този вид терапия се препоръчва и предписването на така наречените малки невролептици (тиоридазин, хлорпротиксен, сулпирид), чиято психотропна активност се състои в ефект върху проявите на депресивния полюс и безсъние.
- Преодоляване на терапевтичната резистентност към атипични антипсихотици при лечение на остри психотични състояния. За тази цел обикновено се използват парентерални форми на традиционни антипсихотици с глобално (хлорпромазин, левомепромазин и др.) и селективно (халоперидол) антипсихотично действие.
Тези лекарства причиняват различни странични ефекти, чийто характер зависи от характеристиките на фармакологичния профил на всяко лекарство. Антипсихотиците с по-изразен холинолитичен ефект по-често причиняват нарушения на акомодацията, запек, сухота в устата и задържане на урина. Седативният ефект е по-характерен за антипсихотиците с изразен антихистаминов ефект, а ортостатичната хипотония е по-характерна за лекарства, които блокират α1-адренергичните рецептори. Блокирането на холинергичното, нордренергическото и допаминергичното предаване от типичните невролептици може да доведе до редица нарушения в сексуалната сфера, като аменорея или дисменорея, аноргазмия, галакторея, подуване и болезненост на млечните жлези и намалена потентност. Страничните ефекти в сексуалната сфера са свързани главно с холинолитичните и адреноблокиращите свойства на тези лекарства, както и с повишаване на секрецията на пролактин поради блокиране на метаболизма на допамина. Най-сериозните странични ефекти на типичните невролептици са двигателната дисфункция. Те са най-честата причина пациентите да спрат приема на лекарства. Трите основни странични ефекта на терапията, свързани с влиянието върху двигателната сфера, включват ранни екстрапирамидни синдроми, тардивна дискинезия и НМС.
Смята се, че екстрапирамидните синдроми са свързани с блокиране на D2 рецепторите в базалните ганглии. Те включват дистония, невролептичен паркисонизъм и акатизия. Проявите на остра дистонична реакция (ранна дискинезия) включват внезапно развиваща се хиперкинеза, окулогирни кризи, контракции на мускулите на лицето и торса, опистотонус. Тези нарушения са дозозависими и често се появяват след 2-5 дни терапия с високоефективни невролептици като халоперидол и флуфеназин. За облекчаване на ранната дискинезия, дозата на невролептиците се намалява и се предписват антихолинергични лекарства (бипериден, трихексифенидил). Тардивната дискинезия обикновено засяга мускулите на врата и, за разлика от острата дистонична реакция, е по-слабо чувствителна към лечение с антихолинергици. Невролептичният паркисонизъм се характеризира с намалена спонтанна моторика, хипо- и амимия, тремор в покой и ригидност. Важно е да се разграничат тези симптоми от външно подобните негативни разстройства при шизофрения, които се представят с емоционално отчуждение, притъпяване на афекта и анергия. За коригиране на тези странични ефекти е показано прилагането на антихолинергици, намаляване на дозата на невролептика или замяната му с атипичен антипсихотик. Акатизията се проявява с вътрешна тревожност, невъзможност за дълго време на едно място и необходимост от постоянно движение на ръцете или краката. За облекчаването ѝ се използват антихолинергици и централни бета-блокери (пропранолол).
Късната дискинезия се проявява с неволеви движения на всяка мускулна група, най-често мускулите на езика и устата. Клинично се разграничават редица нейни форми: дискинезия на мускулите на бузите, езика, устата (периодични контракции на дъвкателните мускули, създаващи впечатление за гримасиращо лице, езикът може неволно да се подава от устата на пациента); тардивна дистония и тардивна акатизия; (пациентът прави хореоатетоидни движения на главата, торса, горните и долните крайници). Тази форма на разстройство се регистрира главно по време на продължително лечение с традиционни невролептици и се открива при приблизително 15-20% от пациентите, приемащи ги като поддържаща терапия. Вероятно при някои пациенти рискът от развитие на симптоми на дискинезия е повишен, тъй като някои от тях са наблюдавани в клиниката на шизофренията още преди „невролептичната ера“. Освен това, тардивна дискинезия е описана при възрастни жени и пациенти с афективни разстройства. Смята се, че тардивната дискинезия е свързана с увеличаване на броя на допаминовите рецептори в стриатума, въпреки че е вероятно GABAergic и други невротрансмитерни системи също да участват в нейната патогенеза. Няма ефективно универсално лечение за такива странични ефекти. Предполага се, че ниски дози високоефективни невролептици с допаминов блокиращо действие или витамин Е могат да имат умерен благоприятен ефект при тези нарушения. Най-ефективната мярка за тардивна дискинезия е намаляване на дозата на типичен невролептик или замяната му с атипичен антипсихотик.
Според съвременните данни, невролептичният малигнен синдром се среща в приблизително 0,5% от случаите на психофармакотерапия. Вероятно рядката поява на такова животозастрашаващо усложнение в момента може да се обясни с широкото въвеждане на атипични антипсихотици в практиката, тъй като рискът от развитие на НМС по време на лечение с тези лекарства е незначителен. Общоприето е, че основната причина за развитието на НМС е прекомерното блокиране на допаминергичната система по време на терапия с невролептици, особено след увеличаване на дозата на силно мощен антипсихотик. Основните симптоми на НМС са хипертермия, повишен тонус на скелетните мускули и сухожилни рефлекси, нарушено съзнание с преход в кома. Кръвните изследвания разкриват левкоцитоза, повишена скорост на утаяване на еритроцитите, повишена активност на чернодробните трансаминази; изследванията на урината разкриват наличие на албуминурия. Нарушенията на водно-електролитния баланс настъпват бързо, което създава предпоставки за образуване на мозъчен оток. НМС е остро състояние, изискващо спешна хоспитализация на пациента за интензивна инфузионна терапия. При лечението на НМС най-важни са хидратацията и симптоматичната терапия. В тази ситуация всички предписани невролептици изискват незабавно спиране на приема. В някои случаи, агонисти на допаминовите рецептори (например бромокриптин) или мускулни релаксанти имат положителен ефект, въпреки че тяхната ефективност не е проучена. След елиминиране на НМС, невролептикът не трябва да се възобновява поне две седмици. Впоследствие може да се предпише антипсихотик с ниска потентност, за предпочитане лекарство от ново поколение. Дозата на новопредписаното лекарство трябва да се увеличава изключително внимателно, като се следи състоянието на жизнените функции и лабораторните данни (кръвни и уринни изследвания).
Типичните невролептици рядко причиняват опасни фатални усложнения. Проявите на предозиране са свързани главно с индивидуалния профил на антиадренергичното и антихолинергичното действие на лекарството. Тъй като тези лекарства имат силен антиеметичен ефект, за елиминирането им от организма е показана стомашна промивка, а не прилагане на еметици. Артериалната хипотония, като правило, е следствие от блокада на адренергичните рецептори и трябва да се коригира чрез прилагане на допамин и норепинефрин. В случай на сърдечна аритмия е показано прилагането на лидокаин.
Механизъм на действие и фармакологични ефекти на типичните антипсихотици
С развитието на психофармакологията бяха предложени различни варианти за ефекта на антипсихотиците върху неврорецепторите. Основната хипотеза остава, че те засягат допаминовите невроструктури (предимно D2 рецепторите), въз основа на данни за нарушаване на нормалния метаболизъм на допамина в мозъчните структури при психози. Допаминовите D2 рецептори са разположени в базалните ганглии, nucleus accumbens и фронталната кора; те играят водеща роля в регулирането на потока от информация между мозъчната кора и таламуса.
Фигурата демонстрира по-детайлно разбиране на нарушенията в предаването на допамин в кортикалните и подкорковите области на мозъка и ролята на тези нарушения в развитието на симптомите на шизофрения (адаптирано от монографията на Jones RB, Buckley PF, 2006).
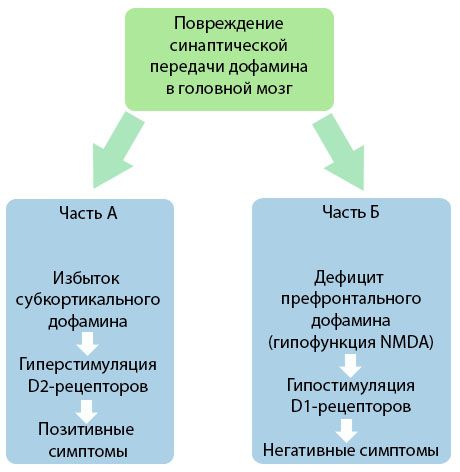
Част А отразява класическата, ранна допаминова теория, постулираща излишък на допамин в подкорковите области и хиперстимулация на D2 рецепторите, което води до появата на продуктивни симптоми. Част Б демонстрира последващата модернизация на теорията в началото на 90-те години на миналия век. Данните, получени по това време, разкриват, че дефицитът на допамин в D рецепторите, заедно с недостатъчната стимулация на тези рецептори в префронталния кортекс, води до появата на негативни симптоми и когнитивни дефицити. Следователно, според съвременните разбирания, и двата вида нарушения на допаминергичното предаване - излишък на подкорков допамин и неговият дефицит в префронталния кортекс - са комбиниран резултат от нарушаване на синаптичното предаване в префронталната област и са свързани с хипофункция на N-метил-N-аспартат. В допълнение към първоначално изолирания допамин, по-късно са идентифицирани и други невротрансмитери, участващи в патогенезата на шизофренията, като серотонин, гама-аминомаслена киселина, глутамат, норепинефрин, ацетилхолин и различни невропептиди. Въпреки че ролята на тези медиатори не е напълно проучена, въпреки това, с развитието на знанията, става ясно, че проявата на множество неврохимични промени в организма е свързана с това. Следователно, клиничният ефект на антипсихотично лекарство е сумиране на ефектите върху различни рецепторни образувания и води до елиминиране на нарушенията на хомеостазата.
През последните години, благодарение на появата на нови методи за изследване, като например свързване на радиоизотопни лиганди и PET сканиране, е постигнат значителен напредък в изясняването на финия биохимичен механизъм на действие на невролептиците. По-специално, е определена сравнителната сила и тропизъм на лекарствата да се свързват с отделни неврорецептори в различни области и структури на мозъка. Показана е пряка зависимост на тежестта на антипсихотичния ефект на лекарството от силата на блокиращия му ефект върху различни допаминергични рецептори. Наскоро бяха идентифицирани четири вида такива рецептори:
- D1 са разположени предимно в областта на substantia nigra и стриатума (т.нар. нигростриатална област), както и в префронталната област;
- D2 - в нигростриаталната, мезолимбичната област и предната хипофизна жлеза (секреция на пролактин);
- D3 (пресинаптичен) - в различни мозъчни структури, контролира допаминергичната активност съгласно закона за отрицателната обратна връзка;
- D4 (пресинаптичен) - предимно в нигростриаталната и мезолимбичната области.
Същевременно вече може да се счита за доказано, че именно блокадата на D2 рецепторите причинява развитието на антипсихотични, вторични седативни ефекти, както и екстрапирамидни странични ефекти. Други клинични прояви на блокадата на този тип рецептори са аналгетичният и антиеметичният ефект на невролептиците (намаляване на гаденето, повръщането в резултат на потискане на центъра за повръщане), както и намаляване на съдържанието на растежен хормон и увеличаване на производството на пролактин (невроендокринни странични ефекти, включително галакторея и менструални нарушения). Дългосрочната блокада на нигростриаталните D2 рецептори води до появата на тяхната свръхчувствителност, която е отговорна за развитието на тардивни дискинезии и „психози на свръхчувствителност“. Вероятните клинични прояви на блокадата на пресинаптичните D3 и D4 рецептори са свързани главно със стимулиращия ефект на невролептиците. Поради частичното блокиране на тези рецептори в нигростриаталната и мезолимбокортикалната области, активиращите и инцизивни (мощни, високоактивни) невролептици в малки дози могат да стимулират, а във високи дози да потискат допаминергичното предаване.
През последните години интересът към функцията на серотонинергичните системи на мозъка, включително серотониновите рецептори, рязко се увеличи. Факт е, че в различни части на мозъка серотонинергичната система има модулиращ ефект върху допаминергичните структури. По-специално, в мезокортикалната област серотонинът инхибира освобождаването на допамин и съответно блокадата на постсинаптичните 5-HT рецептори води до повишаване на съдържанието на допамин. Както е известно, развитието на негативни симптоми при шизофрения е свързано с хипофункция на допаминовите неврони в префронталните структури на мозъчната кора. В момента са известни около 15 вида централни 5-HT рецептори. Експериментално е установено, че невролептиците се свързват главно с 5-HT рецепторите от първите три типа.
Тези лекарства имат предимно стимулиращ (агонистичен) ефект върху 5-HT1a рецепторите. Вероятни клинични последици: повишена антипсихотична активност, намалена тежест на когнитивните нарушения, коригиране на негативните симптоми, антидепресивен ефект и намалена честота на екстрапирамидни странични ефекти.
Ефектът на невролептиците върху 5-HT2 рецепторите, особено върху 5-HT2a подтиповете, е от съществено значение. Те са разположени главно в мозъчната кора и чувствителността им е повишена при пациенти с шизофрения. Способността на невролептиците от ново поколение да намаляват тежестта на негативните симптоми, да подобряват когнитивните функции, да регулират съня чрез увеличаване на общата продължителност на бавно-вълновите (D-вълнови) етапи на съня, да намаляват агресията и да облекчават депресивните симптоми и мигреноподобните (възникващи от мозъчно-съдови нарушения) главоболия се свързва с блокадата на 5-HT2a рецепторите. От друга страна, при блокадата на 5-HT2a рецепторите са възможни хипотензивни ефекти и нарушения на еякулацията при мъжете.
Смята се, че ефектът на невролептиците върху 5-HT2c рецепторите причинява седативен (анксиолитичен) ефект, повишен апетит (придружен от увеличаване на телесното тегло) и намаляване на производството на пролактин.
5-HT3 рецепторите са разположени предимно в лимбичната област и когато са блокирани, първо се развива антиеметичният ефект, а антипсихотичните и анксиолитичните ефекти също се засилват.
Появата на симптоми, подобни на паркинсонизъм, зависи и от блокиращата сила на лекарството върху мускариновите холинергични рецептори. Холинолитичните и допаминовите блокиращи ефекти са до известна степен в реципрочни зависимости. Известно е например, че в нигростриаталната област D2 рецепторите инхибират освобождаването на ацетилхолин. Когато повече от 75% от D2 рецепторите в нигростриаталната област са блокирани, балансът се нарушава в полза на холинергичната система. Това е причината за коригиращия ефект на антихолинергичните лекарства (коректори) върху невролептичните екстрапирамидни странични ефекти. Хлорпротиксен, клозапин и оланзапин имат висок афинитет към мускариновите рецептори и практически не предизвикват екстрапирамидни странични ефекти, тъй като блокират едновременно холинергичните и допаминергичните рецептори. Халоперидол и пиперазин фенотиазиновите производни имат изразен ефект върху допаминовите рецептори, но имат много слаб ефект върху холиновите рецептори. Това се дължи на способността им да причиняват изразени екстрапирамидни странични ефекти, които се намаляват при употреба на много високи дози, когато холинолитичният ефект става забележим. В допълнение към намаляването на блокиращия допамина ефект върху D2 рецепторите на нигростриаталната област и изравняването на екстрапирамидните странични ефекти, силният холинергичен ефект може да причини влошаване на когнитивните функции, включително нарушения на паметта, както и периферни странични ефекти (сухи лигавици, нарушена зрителна акомодация, запек, задържане на урина, объркване и др.). Невролептиците имат сравнително силен блокиращ ефект върху хистаминовите рецептори тип I, което е свързано, на първо място, с тежестта на седативния ефект, както и с повишаване на телесното тегло поради повишен апетит. Антиалергичните и антипруритичните ефекти на невролептиците също са свързани с техните антихистаминови свойства.
В допълнение към блокирането на допамина, антисеротонергичните, холинолитичните и антихистаминовите ефекти, повечето невролептици имат адренолитични свойства, т.е. блокират както централните, така и периферните α1-адренорецептори. Адреноблокерите като хлорпромазин и хлорпротиксен имат изразен седативен ефект. Освен това, блокиращият ефект на тези лекарства може да причини невровегетативни странични ефекти (артериална хипотония, тахикардия и др.), както и засилване на хипотензивния ефект на адреноблокерите.
Трудовете на голям брой автори предоставят данни за силата на свързване (афинитет) на отделни невролептици с различни видове неврорецептори.
Въз основа на техния неврохимичен профил на действие, типичните и атипичните антипсихотици, сред преобладаващо използваните в клиничната практика, могат условно да бъдат разделени на шест групи.
Първата група се състои от селективни блокери на D2 и D4 рецепторите (сулпирид, амисудприд, халоперидол и др.) от групите на бензамидните и бутирофеноновите производни. В малки дози, главно поради блокирането на пресинаптичните D4 рецептори, те активират допаминергичното предаване на нервните импулси и имат стимулиращ (дезинхибиторен) ефект, в големи дози блокират D2 рецепторите във всички области на мозъка, което се проявява клинично с изразен антипсихотичен ефект, както и с екстрапирамидни и ендокринни (поради пролактинемия) странични ефекти.
Втората група включва високоактивни D2-рецепторни блокери, както и лекарства, които слабо или умерено блокират 5-HT2a- и 5-HT1a-рецепторите (флупентиксол, флуфеназин, зуклопентиксол и др.), т.е. предимно пиперазинови производни на фенотиазина или тиоксантени, близки до тях по стереохимична структура. Подобно на лекарствата от първата група, тези невролептици имат, на първо място, изразен антипсихотичен (индуциращ) ефект, а също така предизвикват екстрапирамидни пие ефекти и пролактинемия. В малки дози те имат умерено активиращ (психостимулиращ) ефект.
Третата група се състои от поливалентни седативни невролептици, които блокират повечето неврорецептори по недиференциран начин. Тези лекарства имат ясно изразен блокиращ ефект върху допаминовите рецептори, а също така предизвикват силни адренолитични и холинолитични ефекти. Това включва повечето седативни невролептици, предимно алифатни и пиперидинови производни на фенотиазина, както и тиоксантени, които са близки до тях по стереохимична структура (хлорпромазин, левомепромазин, хлорпротиксен и др.). Спектърът на психотропната активност на тези лекарства е доминиран, на първо място, от изразен първичен седативен ефект, развиващ се независимо от използваната доза, и умерен антипсихотичен ефект. Освен това, поради изразения си антихолинергичен ефект, лекарствата от тази група причиняват слаби или умерени екстрапирамидни и невроендокринни странични ефекти, но често водят до развитие на ортостатична хипотония и други автономни реакции поради изразена блокада на a1-адренергичните рецептори.
Четвъртата група включва невролептици, които блокират D2- и 5-HT2a-рецепторите по балансиран начин, т.е. в еднаква степен (последните в малко по-голяма степен) и a1-адренорецепторите в умерена степен. Тази група включва представители на новото поколение атипични антипсихотици (рисперидон, зипразидон, сертиндол), които имат различни химични структури. Неврохимичният механизъм на действие определя тяхното селективно влияние предимно върху мезолимбичните и мезокортикалните области на мозъка. Наред с отчетливия антипсихотичен ефект, липсата или слабата експресия на екстрапирамидни странични ефекти (при използване на терапевтични дози), слабата или умерена пролактинемия и умерените адренолитични свойства (хипотензивни реакции), тази група невролептици е способна да коригира негативните симптоми чрез индиректно стимулиране на допаминергичното предаване в мозъчната кора.
Петата група се състои от поливалентни атипични антипсихотици от трицикличния дибензодиазепин или с подобна структура (клозапин, оланзапин и кветиапин). Точно както лекарствата от третата група, те блокират повечето неврорецептори по недиференциран начин. 5-HT2a рецепторите обаче са блокирани по-силно от D2 и D4 рецепторите, особено тези, разположени в нигростриаталната област. Това определя действителната липса или слаб екстрапирамиден ефект и липсата на невроендокринни странични ефекти, свързани с повишено производство на пролактин с ясно изразен антипсихотичен ефект и способността да намаляват тежестта на негативните симптоми. Освен това, всички лекарства от тази група имат изразени адренолитични и антихистаминови свойства, което определя седативните и хипотензивните ефекти. Клозапин и оланзапин също имат доста изразен блокиращ ефект върху мускариновите рецептори и водят до развитие на холинолитични странични ефекти.
По този начин, способността за блокиране на постсинаптичните допаминергични рецептори с компенсаторно увеличение на синтеза и метаболизма на допамина е единственото общо биохимично свойство за всички невролептици, разглеждани в тези групи.
Шестата група включва единствения атипичен антипсихотик, арипипразол, който се появи на местния психофармакологичен пазар сравнително наскоро. Това лекарство е частичен агонист на D2-допаминовите рецептори и действа като функционален антагонист в хипердопаминергично състояние и като функционален агонист в хиподопаминергичен профил. Такъв уникален рецепторен профил на арипипразол позволява намаляване на риска от екстрапирамидни разстройства и хиперпролактинемия при употребата му. Освен това, арипипразол действа като частичен агонист на 5-HT1a рецепторите и едновременно с това е антагонист на 5-HT2a рецепторите. Предполага се, че подобно взаимодействие с рецепторите води до общо балансирано функциониране на серотониновата и допаминовата система, така че механизмът на действие на арипипразол може да се определи като стабилизиране на допамин-серотониновата система.
По този начин, настоящото ниво на познания за неврохимичните механизми на действие на невролептиците ни позволява да предложим нова, патогенетично по-обоснована фармакодинамична класификация на тази група психотропни лекарства. Използването на тази класификация ни позволява да предвидим до голяма степен спектъра на психотропната активност, толерантността и вероятните лекарствени взаимодействия на дадено лекарство. С други думи, характеристиките на неврохимичната активност на дадено лекарство до голяма степен определят характеристиките на неговата клинична активност, което трябва да се използва при избора на конкретно антипсихотично лекарство за конкретен пациент.
Ефективността на глобалния антипсихотичен ефект на всеки невролептик се оценява с помощта на така наречения хлорпромазинов еквивалент, който се приема за 1. Например, хлорпромазиновият еквивалент на халоперидол = 50. Това означава, че антипсихотичната ефективност на 1 mg халоперидол е сравнима с 50 mg хлорпромазин. Въз основа на този показател е разработена класификация, която предвижда разпределението на невролептици с висока (хлорпромазинов еквивалент > 10,0), средна (хлорпромазинов еквивалент = 1,0-10,0) и ниска (хлорпромазинов еквивалент = 1,0) антипсихотична активност, наречена патентност. Типичните невролептици (антипсихотици от първо поколение) се използват широко в клиничната психофармакотерапия от почти половин век. Спектърът на тяхната терапевтична активност включва:
- глобално антипсихотично действие под формата на способност за равномерно и диференцирано намаляване на различни прояви на психоза:
- първичен седативен (инхибиращ) ефект - способността на лекарствата бързо да облекчават психомоторната възбуда;
- селективно, селективно антипсихотично действие, проявяващо се в способността да се повлиява върху отделни симптоми: делириум, халюцинации, дезинхибиране на влеченията и др.;
- активиращо (дезинхибиторно, дезинхибиторно, антиаутистично) невротропно действие, проявяващо се с развитието на екстрапирамидни симптоми;
- соматотропно действие под формата на развитие на невроендокринни и вегетативни странични ефекти;
- депресивен ефект, изразяващ се в способността на някои антипсихотици да причиняват депресивни симптоми.
Ефективността на антипсихотиците от първо поколение при лечението не само на психотични разстройства, но и на разстройства в рамките на граничната психиатрия е доказана многократно и е безспорна. Следователно, въпреки високата честота на странични ефекти от терапията при предписването им, те продължават да се използват в медицинската практика.
Странични ефекти от антипсихотичната терапия
Таблицата изброява основните странични ефекти на атипичната антипсихотична терапия.
Подготовка |
Екстрапирамидни |
Нарушение на проводимостта на ЕКГ |
Метаболитни нарушения (наддаване на тегло, повишени нива на глюкоза, холестерол, триглицериди в кръвта) |
||
Клозапин |
. |
++ |
++ |
++- |
|
Рисперидон |
++ |
+/- |
++ |
+/- |
|
Оланзапин |
+ |
+/- |
+++ |
++ |
+++ |
Кветиапин |
+/- |
+ |
+/- |
--- |
|
Зипразидон |
+ |
++ |
+/- |
+/- |
+/- |
Сертиндол |
++ |
-- |
+/- |
-- |
|
Арилипразол |
-- |
--- |
+/- |
-- |
-- |
Амисулприд |
++ |
+/- |
|||
Забележка. Тежест на страничните ефекти: "+++" - висока; "++" - средна; "+" - ниска; "+/-" - съмнителна; "-" - липсваща.
Екстрапирамидни синдроми
Една от основните характеристики на атипичните антипсихотици, за разлика от традиционните, е ниската им способност да причиняват екстрапирамидни синдроми, което се превърна в пробив в поддържащата фармакотерапия на шизофренията. Въпреки това, както следва от данните в таблицата, при употреба на отделни лекарства от тази серия (рисперидон, амисулприд) могат да се появят такива симптоми, което изисква специално внимание при предписването им.
 [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
ЕКГ аномалии
Възможността за развитие на сърдечни странични ефекти е сериозен проблем при използването на някои съвременни антипсихотици в терапията. В тези случаи говорим за удължаване на QT интервала, което може да доведе до развитие на аритмия. Проводимите нарушения, предимно удължаване на QT интервала, се наблюдават най-често по време на лечение с клозапин, сертиндол, зипразидон. Съпътстваща патология под формата на брадикардия, атриовентрикуларен блок, хипотиреоидизъм може да допринесе за появата на това усложнение по време на терапия с гореспоменатите лекарства. Понастоящем се препоръчва ЕКГ мониторинг приблизително веднъж на всеки 3 месеца при пациенти, получаващи поддържаща терапия с атипични антипсихотици.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Ендокринни нарушения
В момента най-голямо безпокойство предизвиква способността на атипичните антипсихотични лекарства да причиняват наддаване на тегло. Повишеното телесно тегло, нивата на глюкоза и триглицериди в кръвта могат да доведат до метаболитни нарушения и развитие на диабет тип 2. Необходими са особено внимание и седмично наблюдение на биохимичните параметри по време на терапия с клозапин и оланзапин. Според J. Geddes et al. (2000), PB Jones, PF Buckley (2006), трябва да се признае за целесъобразно провеждането на щателен преглед на пациентите, преди да им се предпише определен антипсихотик от съвременното поколение, тъй като е известно, че метаболитните нарушения се срещат по-често при пациенти, които са имали наследствена предразположеност, наднормено телесно тегло, нарушения на липидния спектър и хипергликемия преди началото на лечението. Алгоритъмът за наблюдение, предложен от PB Jones, PF Buckley (2006), включва няколко точки.
- Събиране на медицинска анамнеза и семейни фактори относно риска от метаболитни нарушения.
- Регистрация на индекс на телесна маса, ЕКГ, кръвно налягане и пулс преди започване на лечението.
- Събиране на лабораторни данни (глюкоза, липиден профил, холестерол) преди започване на терапия.
- Редовно наблюдение на индекса на телесна маса и жизнените показатели по време на лечението.
- Мониторинг на лабораторните данни по време на лечението.
Появата на хиперпролактинемия по време на антипсихотична терапия се дължи на централно блокиране на допаминовите рецептори в хипоталамуса, което води до освобождаване на пролактин от предната хипофизна жлеза. Хиперпролактинемията най-често се проявява при лечение с оланзапин, рисперидон и амисулприд.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Агранулоцитоза
Друго сериозно усложнение на антипсихотичната терапия. Може да се наблюдава по време на лечение с клозапин и оланзапин. Според J. Geddes et al. (2000), то е диагностицирано през първите 3 месеца при 1-2% от пациентите, приемащи тези лекарства. В тази връзка се препоръчват седмични кръвни изследвания за пациенти, приемащи тези лекарства през първите 18 седмици от терапията, и месечно наблюдение след това. Доказано е, че когато дозата на гореспоменатите невролептици се намали, клиничните кръвни изследвания се връщат към нормалното. Същевременно трябва да се признае, че към днешна дата няма ясна стратегия за пациенти, които изпитват гореспоменатите странични ефекти, свързани с метаболитни нарушения. Най-често един атипичен антипсихотик се заменя с друг. Друга обещаваща насока е назначаването на специална коригираща терапия, по-специално използването на бромокриптин за коригиране на хиперпролактинемията. Идеалната ситуация е тази, при която грижите за пациент с такива нарушения се осъществяват с периодичното участие на интернисти, по-специално ендокринолози, кардиолози и други специалисти.
В заключение следва да се отбележи, че ако се спазват дадените алгоритми за предписване и наблюдение не само на психическото, но и на физическото състояние на пациентите, употребата на лекарства от второ поколение е по-безопасна от типичните невролептици.
Редица други антипсихотици са в етап на разработка. Лекарствата от следващо поколение вероятно ще имат различен механизъм на действие (например, GABAергичен профил) и ще могат да повлияят на различни прояви на шизофрения, включително самите дефицитни разстройства.
Атипични антипсихотици
Съвременните насоки съдържат данни за предимствата на използването на антипсихотици от второ поколение във фармакотерапията. Терминът „атипичен“ (синоним - антипсихотици от второ поколение) е условен и се използва главно за удобство при обозначаване на новото поколение. В сравнение с традиционните невролептици, лекарствата от тази група са по-ефективни при коригиране на негативни, афективни и когнитивни разстройства, което е съчетано с по-добра поносимост и по-нисък риск от екстрапирамидни симптоми. Разликите в характера на терапевтичния ефект на едно или друго лекарство от серията атипични антипсихотици се обясняват, както и в групата на типичните невролептици, с неговия индивидуален профил на фармакологично действие.
За да се изяснят възможностите на психофармакотерапията с атипични антипсихотици, е препоръчително да се съсредоточим върху лекарствата от тази група, регистрирани в Русия.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Клозапин (дибензодиазепин)
Основател на групата атипични антипсихотици. Механизмът на действие на клозапин се характеризира с леко блокиране на D2 рецепторите с едновременен висок антагонизъм към 5-HT2a рецепторите, a1, a2-адренергичните и H1-хистаминовите рецептори. Той се е доказал като ефективен антипсихотик в случаи на резистентност към други антипсихотици (лекарство от резервната група), а също така е показан за лечение на хронична мания, психотична възбуда, агресия. В домашната практика клозапин често се предписва за постигане на седация и като хипнотик при психотични пациенти. Трябва да се признае, че подобна употреба на клозапин не съответства на основния му профил на показания за употреба в терапията. Вероятно отношението към този антипсихотик като лекарство с второстепенно значение трябва да се преразгледа, тъй като днес той е единственото лекарство с доказана ефективност при резистентни пациенти.
Клозапин, за разлика от типичните невролептици, не причинява сериозни екстрапирамидни нарушения поради гореспоменатия нисък афинитет към О2 рецепторите. Оказа се също, че може да се използва за лечение на късна дистония и тежка акатизия. Поради ниския риск от развитие на НМС, клозапин може да се счита за лекарство по избор при пациенти, които преди това са страдали от това усложнение.
Въпреки това, по време на терапия с клозапин могат да се развият редица сериозни странични ефекти. Най-опасният от тях (дори когато се предписват малки дози) е агранулоцитозата, която се среща при 0,5-1,0% от пациентите. Други важни странични ефекти, които могат да възникнат при употреба на лекарството, включват сънливост, хиперсаливация и наддаване на тегло, което често вече е повишено към момента на предписване на клозапин под влиянието на предишна антипсихотична терапия. Трябва да се обърне внимание и на възможността за развитие на тахикардия, артериална хипотония и епилептични припадъци по време на приема му. Вероятността от припадъци зависи от дозата. Рискът им се увеличава значително, ако дозата клозапин надвиши 600 mg/ден. Развитието на припадъци не е противопоказание за по-нататъшна употреба на лекарството, но изисква намаляване наполовина на дозата и предписване на антиконвулсанти, като валпроева киселина. Превенцията на страничните ефекти от лечението с клозапин включва внимателно наблюдение на броя на белите кръвни клетки, както и на ЕКГ и ендокринните параметри.
Предозирането с клозапин може да причини потискане на съзнанието до развитие на кома, както и симптоми, свързани с холинолитичния ефект (тахикардия, делириум), епилептични припадъци, респираторна депресия, екстрапирамидни синдроми. Фатален изход може да настъпи при прием на доза над 2500 mg от лекарството.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
Рисперидон
Бензизоксазолово производно с висок афинитет към серотонинови и допаминови Dj рецептори с преобладаващ ефект върху серотониновата система. Лекарството има широк спектър от показания за употреба, включително облекчаване на обостряния, лечение против рецидиви, терапия на първия психотичен епизод и коригиране на негативните симптоми на шизофрения. Доказано е, че лекарството подобрява когнитивните функции при пациенти с шизофрения. Получени са предварителни данни, че рисперидонът също така намалява съпътстващите афективни симптоми при пациенти с шизофрения и може да бъде лекарство по избор при лечението на биполярни афективни разстройства.
Страничните ефекти от терапията с рисперидон, особено екстрапирамидните нарушения, са дозозависими и се появяват по-често при дози над 6 mg/ден. Други странични ефекти включват гадене, повръщане, тревожност, сънливост и повишени серумни нива на пролактин. Дългосрочната употреба на рисперидон може да доведе до наддаване на тегло и развитие на захарен диабет тип 2, но с по-малка вероятност в сравнение с клозапин, оланзапин.
Предозирането може да причини сънливост, епилептични припадъци, удължаване на QT интервала и разширяване на QRS комплекса, както и артериална хипотония. Описани са случаи на фатален изход поради предозиране с рисперидон.
Безспорно предимство на лекарството е наличието на течни и бързоразтворими (сублингвални) форми, чието приложение ускорява навлизането на лекарството в тялото на пациента и улеснява контрола върху приема му. Съществува и удължена форма на лекарството - прах за приготвяне на суспензия за интрамускулно приложение (конста-рисперидон в микросфери). Препоръчва се за поддържащо лечение на пациенти с шизофрения, особено при пациенти с лошо спазване на режима на лечение. Необходимо е да се вземе предвид фактът, че лекарството се нуждае от около три седмици, за да навлезе в кръвния поток, следователно, когато започва терапия с конста-рисперидон, пациентът трябва допълнително да приема пероралната форма на рисперидон поне 3 седмици след първата инжекция.
Оланзапин
По отношение на фармакологичното действие, той е близък до клозапин, тъй като има плеоморфен рецепторен профил със значителен афинитет към серотонинови, мускаринови, α1-адренергични и хистаминови рецептори. Терапевтичната активност на оланзапин има характеристики, подобни на ефективността на клозапин и рисперидон по отношение на въздействието върху позитивните, негативните и депресивните симптоми на шизофрения. Същевременно са получени данни за по-голямата ефективност на оланзапин в сравнение с други атипични антипсихотици при пациенти с първи психотичен епизод и при корекция на показателите на когнитивното функциониране. Трябва да се има предвид, че в началото на терапията с таблетната форма на лекарството може да се появи бърз дезинхибиторен ефект с повишена психомоторна възбуда и тревожност. Следователно, при лечение на пристъпи, съпроводени с тежка психомоторна възбуда, е показано използването на инжекционната форма на лекарството.
Оланзапин рядко причинява екстрапирамидни нарушения или тардивна дискинезия, а най-честите странични ефекти при употребата му са метаболитни нарушения и наддаване на тегло. Установено е, че пациентите, получаващи оланзапин, доста често изпитват повишени нива на холестерол, плазмени липиди и предразположеност към захарен диабет тип 2, но такива ефекти са еднакво чести при пациенти, получаващи както оланзапин, така и клозапин. В същото време са получени данни, показващи, че наддаването на тегло корелира с положителен отговор към оланзапин (т.е. служи като важен прогностичен индикатор за терапията) и се развива в затлъстяване само при 20-30% от пациентите, които са наддали наднормено тегло по време на лечението.
Предозирането може да причини седация, токсични антихолинергични ефекти, епилептични припадъци и артериална хипотония. Понастоящем няма убедителни данни за оценка на риска от смърт от предозиране.
Кветиапин
Класифицира се като дибензотиазепиново съединение. Рецепторният му профил е до голяма степен подобен на този на клозапин. Нивото на свързване на кветиапин с D2 рецепторите е ниско (по-малко от 50%) и краткотрайно, дори при използване на високи дози. Лекарството е ефективно при лечението на позитивни, негативни и общи симптоми на шизофрения. Има данни за успешното му приложение както в случаи на висока резистентност към терапия, така и за подобряване на когнитивните функции на пациентите, което дава право да се препоръчва като антипсихотик от първа линия за поддържаща терапия на шизофрения. И накрая, кветиапин има умерен антидепресивен, активиращ ефект. Поради това е показан при лечението на депресивно-налудни атаки и разстройства от сенесто-хипохондричния кръг.
Установената висока тимотропна активност на кветиапин обяснява факта, че той е регистриран като средство за облекчаване и вторична профилактика на депресивни разстройства. За лечение на манийни епизоди в рамките на биполярни разстройства от тип I и II, кветиапин се използва като допълнително средство. Липсата на инжекционни форми донякъде ограничава употребата му при пациенти с възбуда и агресивно поведение.
Кветиапин се понася добре, практически не предизвиква екстрапирамидни синдроми, освен в случаите, когато се използват максимални дози. Кветиапин не причинява хиперпролактинемия, по-рядко от оланзапин и клозапин води до наддаване на тегло и нарушен глюкозен толеранс.
Зипразидон
Има уникален профил на рецепторна активност. Като мощен антагонист на 5HT2a рецепторите и D2 рецепторите, той е и активен инхибитор на обратното захващане на серотонин и норепинефрин. Клиничните проучвания са показали значително превъзходство на зипразидон в ефекта му върху психотичните симптоми и проявите на агресия в сравнение с халоперидол. Има и данни за положителния ефект на зипразидон върху когнитивните функции на пациенти с шизофрения, както и върху съпътстващите афективни симптоми, показатели за социално функциониране. Зипразидон обикновено се понася добре и много рядко причинява екстрапирамидни синдроми, наддаване на тегло и метаболитни нарушения. По-често се наблюдава удължаване на QT интервала над 460 ms, поради което е препоръчително пациентите, приемащи това лекарство, да преминат ЕКГ изследване както преди предписване на лекарството, така и да се наблюдават по време на лечението. Особено внимание трябва да се обърне на съпътстващата терапия (прием на антиаритмични лекарства), която може да влоши удължаването на QT интервала и да доведе до развитие на сърдечна аритмия, камерно мъждене.
Сертиндол
Принадлежи към производни на фенилиндол. Има висок функционален антагонизъм по отношение на D2-, серотонинови (особено 5-HT2a-рецептори) и a1-адренергични рецептори. Според електроневрохимични изследвания, сертиндол селективно инхибира допаминовите рецептори във вентралната сегментна област. Такава селективност, по всяка вероятност, осигурява нисък риск от екстрапирамидни синдроми и хиперпролактинемия при употреба на лекарството. Резултатите от сравнителни изследвания показват, че сертиндол е сравним с халоперидол по отношение на антипсихотичната активност. Лекарството има изразен дезинхибиторен ефект при пациенти с негативни и депресивни симптоми, който превъзхожда подобен ефект на рисполепт. Има и доказателства, потвърждаващи ефективността на сертиндол за коригиране на когнитивни нарушения при пациенти с шизофрения. Сертиндолът обикновено се понася добре от пациентите, рядко причинява седация и затова се препоръчва като заместващо лекарство, когато се появят странични ефекти по време на терапия с други съвременни антипсихотици.
Сериозните странични ефекти включват способността на лекарството да удължава QT интервала, което може да доведе до сърдечна аритмия. При анализ на постмаркетингови проучвания стана ясно, че сърдечният профил на сертиндол не се различава от този на други антипсихотици от ново поколение.
Арипипразол
Той има антипсихотична активност, сравнима с други атипични средства, но има по-голям ефект върху параметрите на когнитивното функциониране на пациенти с шизофрения. Гореспоменатото уникално фармакологично действие на лекарството - частичен агонист на D2 рецепторите - позволява да се намали рискът от екстрапирамидни синдроми и хиперпролактинемия при употребата му.
 [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
[ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
Амисулприд
Принадлежи към класа на заместените бензамиди. Лекарството селективно се свързва с подтиповете D2 и D3 допаминергични рецептори, няма афинитет към подтиповете D1, D4 и D5, както и към серотонин, H1-хистаминови, a1-адренергични и холинергични рецептори. При приложение във високи дози блокира постсинаптичните D2 рецептори. В ниски дози дезинхибиторният му ефект се проявява чрез блокиране на пресинаптичните D2, D3 рецептори, поради което употребата му е ефективна и при лечение на негативни симптоми, въпреки че не е комбиниран антагонист на D2 рецепторите и серотониновите рецептори. Резултатите от редица проучвания показват изразена антипсихотична активност на лекарството при приложение във високи дози, която превъзхожда традиционните лекарства.
 [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
[ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
