Медицински експерт на статията
Нови публикации
Синтез, секреция и метаболизъм на катехоламини
Последно прегледани: 06.07.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
Надбъбречната медула произвежда съединения със структура, която е далеч от стероидите. Те съдържат 3,4-дихидроксифенил (катехол) ядро и се наричат катехоламини. Те включват адреналин, норадреналин и допамин бета-хидрокситирамин.
Последователността на синтеза на катехоламини е съвсем проста: тирозин → дихидроксифенилаланин (DOPA) → допамин → норепинефрин → адреналин. Тирозинът постъпва в организма с храната, но може да се образува и от фенилаланин в черния дроб под действието на фенилаланин хидроксилаза. Крайните продукти на превръщането на тирозина в тъканите са различни. В надбъбречната медула процесът протича до етапа на образуване на адреналин, в окончанията на симпатиковите нерви - норепинефрин, в някои неврони на централната нервна система синтезът на катехоламини завършва с образуването на допамин.
Превръщането на тирозин в DOPA се катализира от тирозин хидроксилаза, чиито кофактори са тетрахидробиоптерин и кислород. Смята се, че този ензим ограничава скоростта на целия процес на биосинтеза на катехоламини и се инхибира от крайните продукти на процеса. Тирозин хидроксилазата е основната цел на регулаторните ефекти върху биосинтеза на катехоламини.
Превръщането на DOPA в допамин се катализира от ензима DOPA декарбоксилаза (кофактор - пиридоксал фосфат), който е относително неспецифичен и декарбоксилира други ароматни L-аминокиселини. Има обаче индикации за възможността за модифициране на синтеза на катехоламини чрез промяна на активността на този ензим. Някои неврони нямат ензими за по-нататъшното превръщане на допамина и той е крайният продукт. Други тъкани съдържат допамин бета-хидроксилаза (кофактори - мед, аскорбинова киселина и кислород), която превръща допамина в норепинефрин. В надбъбречната медула (но не и в окончанията на симпатиковите нерви) присъства фенилетаноламин - метилтрансфераза, която образува адреналин от норепинефрин. В този случай S-аденозилметионинът служи като донор на метилови групи.
Важно е да се помни, че синтезът на фенилетаноламин-N-метилтрансфераза се индуцира от глюкокортикоиди, навлизащи в медулата от кората през порталната венозна система. Това може да обясни факта, че две различни ендокринни жлези са комбинирани в един орган. Значението на глюкокортикоидите за синтеза на адреналин се подчертава от факта, че клетките на надбъбречната медула, които произвеждат норадреналин, са разположени около артериалните съдове, докато клетките, произвеждащи адреналин, получават кръв главно от венозните синуси, разположени в надбъбречната кора.
Разграждането на катехоламините протича главно под влиянието на две ензимни системи: катехол-О-метилтрансфераза (COMT) и моноаминооксидаза (MAO). Основните пътища на разграждане на адреналина и норадреналина са схематично показани на Фиг. 54. Под влияние на COMT в присъствието на донора на метиловата група S-адренозилметионин, катехоламините се превръщат в норметанефрин и метанефрин (3-O-метилови производни на норадреналина и адреналина), които под влияние на MAO се превръщат в алдехиди и след това (в присъствието на алдехид оксидаза) във ванилилбадемова киселина (VMA), основният продукт на разграждане на норадреналина и адреналина. В същия случай, когато катехоламините първоначално са изложени на MAO, а не на COMT, те се превръщат в 3,4-диоксомадемова алдехид, а след това, под влиянието на алдехид оксидаза и COMT, в 3,4-диоксомадемова киселина и VMC. В присъствието на алкохол дехидрогеназа, от катехоламини може да се образува 3-метокси-4-оксифенилгликол, който е основният краен продукт на разграждането на адреналина и норадреналина в ЦНС.
Разграждането на допамина е подобно, с изключение на това, че неговите метаболити нямат хидроксилна група при бета-въглеродния атом и следователно вместо ванилилбадемова киселина се образува хомованилинова киселина (HVA) или 3-метокси-4-хидроксифенилоцетна киселина.
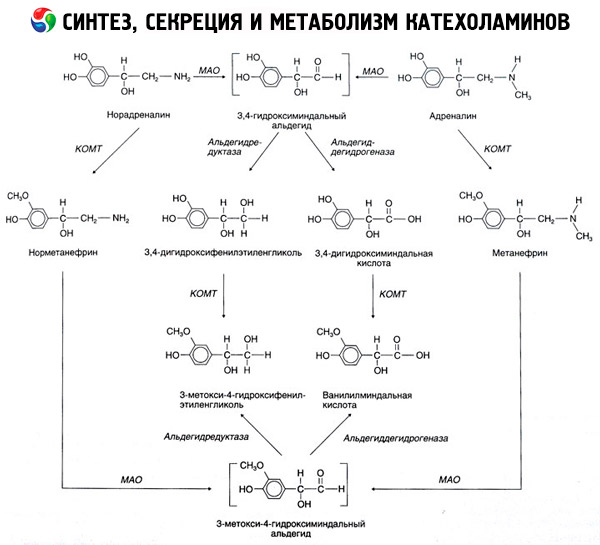
Постулира се също съществуването на хиноиден път на окисление на молекулата на катехоламина, който може да доведе до междинни продукти с изразена биологична активност.
Норепинефринът и адреналинът, образувани под действието на цитозолни ензими в симпатиковите нервни окончания и надбъбречната медула, навлизат в секреторните гранули, което ги предпазва от действието на разграждащите ензими. Улавянето на катехоламини от гранулите изисква разход на енергия. В хромафинните гранули на надбъбречната медула катехоламините са здраво свързани с АТФ (в съотношение 4:1) и специфични протеини - хромогранини, което предотвратява дифузията на хормоните от гранулите в цитоплазмата.
Директният стимул за секрецията на катехоламини очевидно е проникването на калций в клетката, стимулиращо екзоцитозата (сливане на грануларната мембрана с клетъчната повърхност и тяхното разкъсване с пълно освобождаване на разтворимото съдържание - катехоламини, допамин бета-хидроксилаза, АТФ и хромогранини - в извънклетъчната течност).
Физиологични ефекти на катехоламините и техният механизъм на действие
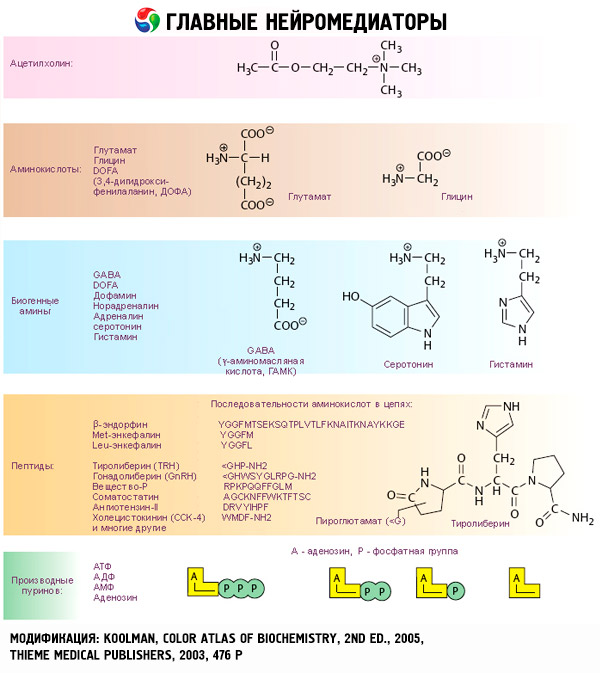
Ефектите на катехоламините започват с взаимодействие със специфични рецептори на целевите клетки. Докато рецепторите за тиреоидни и стероидни хормони са локализирани вътре в клетките, рецепторите за катехоламини (както и за ацетилхолин и пептидни хормони) се намират на външната клетъчна повърхност.
Отдавна е установено, че по отношение на някои реакции, адреналинът или норадреналинът са по-ефективни от синтетичния катехоламин изопротеренол, докато по отношение на други, ефектът на изопротеренола превъзхожда действието на адреналина или норадреналина. На тази основа е разработена концепция за наличието на два вида адренорецептори в тъканите: алфа и бета, като в някои от тях може да присъства само един от тези два вида. Изопротеренолът е най-мощният агонист на бета-адренорецепторите, докато синтетичното съединение фенилефрин е най-мощният агонист на алфа-адренорецепторите. Естествените катехоламини - адреналин и норадреналин - са способни да взаимодействат с рецептори и от двата типа, но адреналинът проявява по-голям афинитет към бета-, а норадреналинът - към алфа-рецепторите.
Катехоламините активират сърдечните бета-адренергични рецептори по-силно от гладкомускулните бета-рецептори, което позволи бета типът да бъде разделен на подтипове: бета1-рецептори (сърце, мастни клетки) и бета2-рецептори (бронхи, кръвоносни съдове и др.). Ефектът на изопротеренола върху бета1-рецепторите надвишава ефекта на адреналина и норадреналина само 10 пъти, докато върху бета2-рецепторите той действа 100-1000 пъти по-силно от естествените катехоламини.
Използването на специфични антагонисти (фентоламин и феноксибензамин за алфа- и пропранолол за бета-рецептори) потвърди адекватността на класификацията на адренорецепторите. Допаминът е способен да взаимодейства както с алфа-, така и с бета-рецептори, но различни тъкани (мозък, хипофизна жлеза, съдове) също имат свои собствени допаминергични рецептори, чийто специфичен блокер е халоперидол. Броят на бета-рецепторите варира от 1000 до 2000 на клетка. Биологичните ефекти на катехоламините, медиирани от бета-рецепторите, обикновено са свързани с активирането на аденилат циклазата и повишаване на вътреклетъчното съдържание на цАМФ. Въпреки че рецепторът и ензимът са функционално свързани, те са различни макромолекули. Гуанозин трифосфат (GTP) и други пуринови нуклеотиди участват в модулацията на активността на аденилат циклазата под влиянието на хормон-рецепторния комплекс. Чрез повишаване на ензимната активност, те изглежда намаляват афинитета на бета рецепторите към агонистите.
Феноменът на повишена чувствителност на денервирани структури е отдавна известен. Напротив, продължителното излагане на агонисти намалява чувствителността на целевите тъкани. Изследването на бета рецепторите е позволило да се обяснят тези явления. Доказано е, че продължителното излагане на изопротеренол води до загуба на чувствителност на аденилат циклазата поради намаляване на броя на бета рецепторите.
Процесът на десенсибилизация не изисква активиране на протеиновия синтез и вероятно се дължи на постепенното образуване на необратими хормон-рецепторни комплекси. Напротив, въвеждането на 6-оксидопамин, който разрушава симпатиковите окончания, е съпроводено с увеличаване на броя на реагиращите бета-рецептори в тъканите. Възможно е повишаването на активността на симпатиковата нервна система да причинява и свързана с възрастта десенсибилизация на кръвоносните съдове и мастната тъкан по отношение на катехоламините.
Броят на адренорецепторите в различни органи може да се контролира от други хормони. Така естрадиолът увеличава, а прогестеронът намалява броя на алфа-адренорецепторите в матката, което е съпроводено със съответно увеличение и намаление на нейния контрактилен отговор към катехоламини. Ако вътреклетъчният „втори посредник“, образуван от действието на бета-рецепторните агонисти, със сигурност е цАМФ, тогава ситуацията по отношение на предавателя на алфа-адренергичните ефекти е по-сложна. Предполага се съществуването на различни механизми: намаляване на нивото на цАМФ, повишаване на съдържанието на цАМФ, модулация на клетъчната калциева динамика и др.
За да се възпроизведат различни ефекти в организма, обикновено са необходими дози адреналин, които са 5-10 пъти по-малки от норадреналина. Въпреки че последният е по-ефективен по отношение на α- и β1-адренорецепторите, важно е да се помни, че и двата ендогенни катехоламина са способни да взаимодействат както с α-, така и с β-рецепторите. Следователно, биологичният отговор на даден орган към адренергично активиране до голяма степен зависи от вида на рецепторите, присъстващи в него. Това обаче не означава, че селективното активиране на нервната или хуморалната връзка на симпатико-надбъбречната система е невъзможно. В повечето случаи се наблюдава повишена активност на различните ѝ връзки. По този начин е общоприето, че хипогликемията рефлекторно активира надбъбречната медула, докато понижаването на кръвното налягане (постурална хипотония) е съпроводено главно с освобождаване на норадреналин от окончанията на симпатиковите нерви.
Адренорецептори и ефектите от тяхното активиране в различни тъкани
Система, орган |
Тип адренергичен рецептор |
Реакция |
Сърдечно-съдова система: |
||
Сърце |
Бета |
Повишена сърдечна честота, проводимост и контрактилност |
Артериоли: |
||
Кожа и лигавици |
Алфа |
Намаляване |
Скелетни мускули |
Бета |
Разширяване Свиване |
Коремни органи |
Алфа (още) |
Намаляване |
Бета |
Разширение |
|
Вени |
Алфа |
Намаляване |
Дихателна система: |
||
Мускулите на бронхите |
Бета |
Разширение |
Храносмилателна система: |
||
Стомах |
Бета |
Намалени двигателни умения |
Черва |
Алфа |
Свиване на сфинктерите |
Слезка |
Алфа |
Намаляване |
Бета |
Релаксация |
|
Екзокринен панкреас |
Алфа |
Намалена секреция |
Урогенитална система: |
Алфа |
Свиване на сфинктера |
Пикочен мехур |
Бета |
Релаксация на изхвъргателния мускул |
Мъжки гениталии |
Алфа |
Еякулация |
Очи |
Алфа |
Разширяване на зеницата |
Кожа |
Алфа |
Повишено изпотяване |
Слюнчени жлези |
Алфа |
Екскреция на калий и вода |
Бета |
Амилазна секреция |
|
Ендокринни жлези: |
||
Островчета на панкреаса |
||
Бета клетки |
Алфа (още) |
Намалена секреция на инсулин |
Бета |
Повишена секреция на инсулин |
|
Алфа клетки |
Бета |
Повишена секреция на глюкагон |
8-клетъчни |
Бета |
Повишена секреция на соматостатин |
Хипоталамус и хипофизна жлеза: |
||
Соматотрофи |
Алфа |
Повишена секреция на STH |
Бета |
Намалена секреция на STH |
|
Лактотрофи |
Алфа |
Намалена секреция на пролактин |
Тиротрофи |
Алфа |
Намалена секреция на TSH |
Кортикотрофи |
Алфа |
Повишена секреция на АКТХ |
| бета | Намалена секреция на АКТХ | |
Щитовидна жлеза: |
||
Фоликуларни клетки |
Алфа |
Намалена секреция на тироксин |
Бета |
Повишена секреция на тироксин |
|
Парафоликуларни (К) клетки |
Бета |
Повишена секреция на калцитонин |
Паращитовидни жлези |
Бета |
Повишена секреция на ПТХ |
Бъбреци |
Бета |
Повишена секреция на ренин |
Стомах |
Бета |
Повишена секреция на гастрин |
БХ |
Бета |
Повишена консумация на кислород |
Черен дроб |
? |
Повишена гликогенолиза и глюконеогенеза с освобождаване на глюкоза; повишена кетогенеза с освобождаване на кетонни тела |
Мастна тъкан |
Бета |
Повишена липолиза с освобождаване на свободни мастни киселини и глицерол |
Скелетни мускули |
Бета |
Повишена гликолиза с освобождаване на пируват и лактат; намалена протеолиза с намаляване на освобождаването на аланин, глутамин |
Важно е да се вземе предвид, че резултатите от интравенозното приложение на катехоламини не винаги адекватно отразяват ефектите на ендогенните съединения. Това се отнася главно за норепинефрина, тъй като в организма той се освобождава предимно не в кръвта, а директно в синаптичните цепки. Следователно, ендогенният норепинефрин активира например не само съдовите алфа рецептори (повишено кръвно налягане), но и бета рецепторите на сърцето (учестена сърдечна честота), докато въвеждането на норепинефрин отвън води главно до активиране на съдовите алфа рецептори и рефлекторно (чрез вагуса) забавяне на сърдечния ритъм.
Ниските дози адреналин активират главно бета рецепторите на мускулните съдове и сърцето, което води до намаляване на периферното съдово съпротивление и увеличаване на сърдечния дебит. В някои случаи първият ефект може да преобладава и след прилагането на адреналин се развива хипотония. При по-високи дози адреналинът активира и алфа рецепторите, което е съпроводено с повишаване на периферното съдово съпротивление и на фона на повишаване на сърдечния дебит води до повишаване на артериалното налягане. Въпреки това, ефектът му върху съдовите бета рецептори също се запазва. В резултат на това повишаването на систоличното налягане надвишава подобния показател на диастоличното налягане (повишаване на пулсовото налягане). С въвеждането на още по-високи дози, алфа-миметичните ефекти на адреналина започват да преобладават: систоличното и диастоличното налягане се повишават паралелно, както под влияние на норепинефрин.
Ефектът на катехоламините върху метаболизма се състои от техните директни и индиректни ефекти. Първите се реализират главно чрез бета рецепторите. По-сложни процеси са свързани с черния дроб. Въпреки че повишената чернодробна гликогенолиза традиционно се счита за резултат от активиране на бета рецепторите, има и доказателства за участие на алфа рецепторите. Индиректните ефекти на катехоламините са свързани с модулация на секрецията на много други хормони, като инсулин. В ефекта на адреналина върху неговата секреция, алфа-адренергичният компонент ясно преобладава, тъй като е доказано, че всеки стрес е съпроводен с инхибиране на секрецията на инсулин.
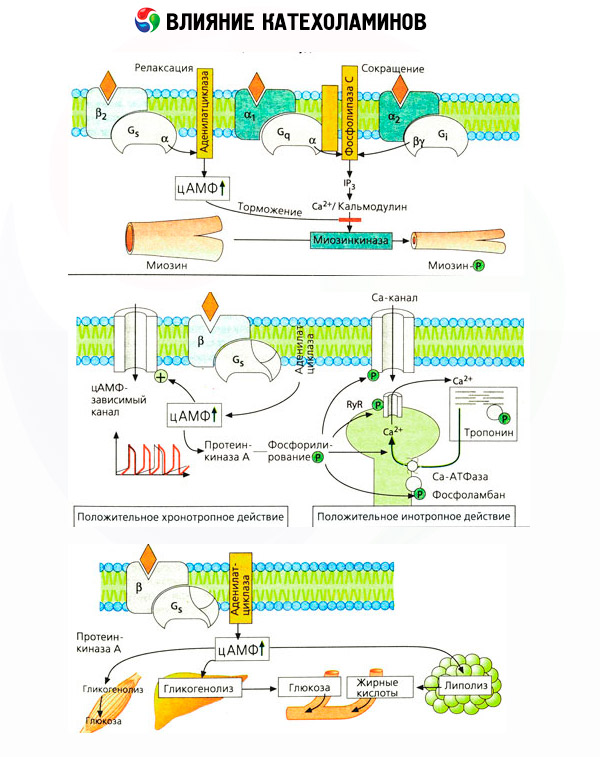
Комбинацията от директни и индиректни ефекти на катехоламините причинява хипергликемия, свързана не само с повишено чернодробно производство на глюкоза, но и с инхибиране на нейното използване от периферните тъкани. Ускоряването на липолизата причинява хиперлипацидемия с повишено доставяне на мастни киселини до черния дроб и засилване на производството на кетонни тела. Повишената гликолиза в мускулите води до увеличаване на освобождаването на лактат и пируват в кръвта, които заедно с глицерол, освободен от мастната тъкан, служат като предшественици на чернодробната глюконеогенеза.
Регулиране на секрецията на катехоламини. Сходството на продуктите и методите на реакция на симпатиковата нервна система и надбъбречната медула е основа за обединяването на тези структури в единна симпатико-надбъбречна система на тялото с разпределението на нейните нервни и хормонални връзки. Различни аферентни сигнали са концентрирани в хипоталамуса и центровете на гръбначния мозък и продълговатия мозък, откъдето произлизат еферентни съобщения, преминаващи към клетъчните тела на преганглионните неврони, разположени в страничните рога на гръбначния мозък на ниво VIII цервикален - II-III лумбален сегмент.
Преганглионните аксони на тези клетки напускат гръбначния мозък и образуват синаптични връзки с неврони, разположени в ганглиите на симпатиковата верига, или с клетки на надбъбречната медула. Тези преганглионни влакна са холинергични. Първата фундаментална разлика между симпатиковите постганглионни неврони и хромафинните клетки на надбъбречната медула е, че последните предават получения от тях холинергичен сигнал не чрез нервна проводимост (постганглионни адренергични нерви), а по хуморалния път, освобождавайки адренергични съединения в кръвта. Втората разлика е, че постганглионните нерви произвеждат норепинефрин, докато клетките на надбъбречната медула произвеждат главно адреналин. Тези две вещества имат различно въздействие върху тъканите.

