Медицински експерт на статията
Нови публикации
Патогенеза на хепатит В
Последно прегледани: 07.07.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
В патогенезата на хепатит В могат да се идентифицират няколко водещи звена в патогенетичната верига:
- въвеждане на патогена - инфекция;
- фиксация върху хепатоцита и проникване в клетката;
- размножаване на вируса и неговото „изтласкване“ върху повърхността на хепатоцита, както и в кръвта;
- активиране на имунологични реакции, насочени към елиминиране на патогена;
- увреждане на органи и системи от имунни комплекси;
- формиране на имунитет, освобождаване от патогена, възстановяване.
Тъй като инфекцията с хепатит B винаги протича парентерално, може да се счита, че моментът на заразяване е практически еквивалентен на проникването на вируса в кръвта. Опитите на някои изследователи да разграничат ентералната и регионалната фаза при хепатит B са слабо обосновани. Има повече основания да се смята, че вирусът веднага навлиза в черния дроб с кръвния поток.
Тропизмът на вируса на хепатит B към чернодробната тъкан е предопределен от наличието на специален рецептор в HBsAg - полипептид с молекулно тегло 31 000 Da (P31), който има албумин-свързваща активност. Подобна албуминова зона се открива и върху мембраната на хепатоцитите в черния дроб на хората и шимпанзетата, което по същество определя тропизма на HBV към черния дроб на хората и шимпанзетата.
Когато вирусът проникне в хепатоцита, се освобождава вирусна ДНК, която, навлизайки в ядрото на хепатоцита и действайки като матрица за синтеза на нуклеинови киселини, задейства серия от последователни биологични реакции, резултатът от които е сглобяването на нуклеокапсида на вируса. Нуклеокапсидът мигрира през ядрената мембрана в цитоплазмата, където се осъществява окончателното сглобяване на частиците на Дейн - пълният вирус на хепатит В.
Трябва да се отбележи обаче, че при инфектиране на хепатоцит процесът може да протече по два начина - репликативен и интегративен. В първия случай се развива картина на остър или хроничен хепатит, а във втория - вирусоносителство.
Причините, които определят двата вида взаимодействие между вирусната ДНК и хепатоцитите, не са точно установени. Най-вероятно видът на реакцията е генетично обусловен.
Резултатът от репликативното взаимодействие е сглобяването на основните антигенни структури (в ядрото) и сглобяването на пълния вирус (в цитоплазмата), последвано от представяне на пълния вирус или неговите антигени върху мембраната или в структурата на хепатоцитната мембрана.
Общоприето е, че репликацията на вируса не води до увреждане на клетките на хепатоцитно ниво, тъй като вирусът на хепатит B няма цитопатичен ефект. Тази позиция не може да се счита за безспорна, тъй като се основава на експериментални данни, които, макар и да показват липсата на цитопатичен ефект на вируса на хепатит B, са получени върху тъканни култури и следователно не могат да бъдат напълно екстраполирани към вирусния хепатит B при хора. Във всеки случай, въпросът за липсата на увреждане на хепатоцитите по време на репликативната фаза изисква допълнително проучване.
Въпреки това, независимо от естеството на взаимодействието на вируса с клетката, черният дроб задължително е включен в имунопатологичния процес. В този случай увреждането на хепатоцитите е свързано с факта, че в резултат на експресията на вирусни антигени върху хепатоцитната мембрана и освобождаването на вирусни антигени в свободна циркулация се включва верига от последователни клетъчни и хуморални имунни реакции, насочени в крайна сметка към отстраняване на вируса от организма. Този процес се осъществява в пълно съответствие с общите модели на имунния отговор към вирусни инфекции. За елиминиране на патогена се включват клетъчни цитотоксични реакции, медиирани от различни класове ефекторни клетки: К-клетки, Т-клетки, естествени убийци, макрофаги. По време на тези реакции заразените хепатоцити се разрушават, което е съпроводено с освобождаване на вирусни антигени (HBcAg, HBeAg, HBsAg), които задействат системата за антителогенезис, в резултат на което в кръвта се натрупват специфични антитела, предимно към ядрото - анти-HBc и e-антиген - анти-HBE. Следователно, освобождаването на чернодробната клетка от вируса се случва в процеса на нейната смърт поради реакциите на клетъчната цитолиза.
В същото време, специфични антитела, натрупващи се в кръвта, се свързват с вирусните антигени, образувайки имунни комплекси, фагоцитирани от макрофаги и екскретирани през бъбреците. В този случай могат да се появят различни имунокомплексни лезии под формата на гломерулонефрит, артериит, артралгия, кожни обриви и др. С участието на специфични антитела, тялото се прочиства от патогена и настъпва пълно възстановяване.
В съответствие с очертаната концепция за патогенезата на хепатит B, цялото разнообразие от клинични варианти на протичане на заболяването обикновено се обяснява с особеностите на взаимодействието на вируса и сътрудничеството на имунокомпетентните клетки, с други думи, силата на имунния отговор към наличието на вирусни антигени. Според съвременните представи силата на имунния отговор е генетично обусловена и е свързана с антигените на хистосъвместимост на HLA локуса от първи клас.
Общоприето е, че при условия на адекватен имунен отговор към вирусни антигени, острият хепатит се развива клинично с цикличен ход и пълно възстановяване. На фона на намаляване на имунния отговор към вирусни антигени, имунно-медиираната цитолиза е незначително изразена, следователно няма ефективно елиминиране на инфектираните чернодробни клетки, което води до леки клинични прояви с дългосрочно персистиране на вируса и евентуално развитие на хроничен хепатит. В същото време, напротив, в случай на генетично обусловен силен имунен отговор и масивна инфекция (хемотрансфузия) възникват обширни области на увреждане на чернодробните клетки, които клинично съответстват на тежки и злокачествени форми на заболяването.
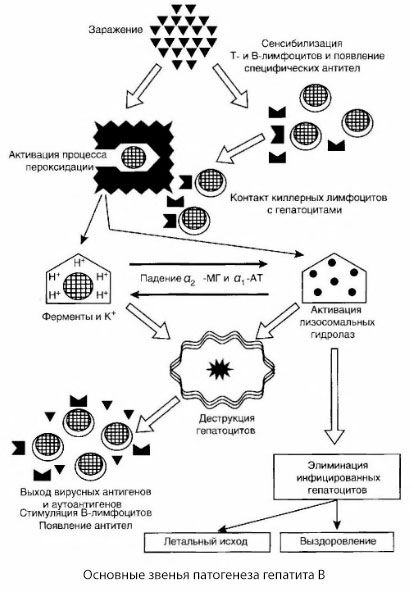
Представената схема на патогенезата на хепатит B се отличава със своята съгласуваност; тя обаче съдържа редица спорни и слабо проучени моменти.
Ако следваме концепцията за хепатит B като имунопатологично заболяване, бихме могли да очакваме увеличаване на клетъчните цитотоксични реакции с нарастваща тежест на заболяването. При тежките форми обаче индексите на клетъчната връзка на имунитета са рязко намалени, включително многократно понижение, в сравнение с тези при здрави деца, и индекса на цитотоксичност на К-клетките. При злокачествената форма, по време на периода на развитие на масивна чернодробна некроза и особено чернодробна кома, се отбелязва пълна неспособност на лимфоцитите за бластна трансформация под влиянието на фитохематутинин, стафилококов ендотоксин и HBsAg. Освен това, няма способност на левкоцитите да мигрират според реакцията на инхибиране на миграцията на левкоцитите (LMIC), а рязко повишаване на пропускливостта на лимфоцитните мембрани се разкрива според резултатите от техните изследвания с помощта на флуоресцентна тетрациклинова сонда.
Така, ако индексите на флуоресценция на лимфоцитите при здрави хора са 9,9±2%, а при типичен хепатит B с доброкачествен ход те се увеличават до 22,3±2,7%, то при злокачествените форми броят на флуоресцентните лимфоцити достига средно 63,5±5,8%. Тъй като повишаването на пропускливостта на клетъчните мембрани недвусмислено се оценява в литературата като надежден индикатор за тяхната функционална непълноценност, може да се заключи, че при хепатит B, особено при злокачествената форма, е налице грубо увреждане на лимфоцитите. Това се доказва и от индексите на цитотоксичност на К-клетките. При тежка форма, на 1-2-рата седмица от заболяването, цитотоксичността е 15,5±8,8%, а при злокачествената форма на 1-вата седмица - 6,0±2,6, на 2-рата - 22,0±6,3% при норма от 44,8±2,6%.
Представените данни ясно показват изразени нарушения в клетъчната връзка на имунитета при пациенти с тежки форми на хепатит В. Очевидно е също, че тези промени настъпват вторично, в резултат на увреждане на имунокомпетентните клетки от токсични метаболити и евентуално циркулиращи имунни комплекси.
Както показват проучванията, при пациенти с тежки форми на хепатит B, особено в случай на развитие на масивна чернодробна некроза, титърът на HBsAg и HBeAg в кръвния серум намалява и едновременно с това започват да се откриват антитела към повърхностния антиген във високи титри, което е напълно нехарактерно за доброкачествените форми на заболяването, при които анти-HBV се появяват едва през 3-тия-5-ти месец от заболяването.
Бързото изчезване на антигените на вируса на хепатит В с едновременната поява на високи титри на антивирусни антитела предполага интензивно образуване на имунни комплекси и евентуалното им участие в патогенезата на развитието на масивна чернодробна некроза.
По този начин, фактическите материали не ни позволяват да интерпретираме хепатит B еднозначно само от гледна точка на имунопатологичната агресия. И въпросът не е само в това, че не се открива връзка между дълбочината и разпространението на морфологичните промени в черния дроб, от една страна, и тежестта на факторите на клетъчния имунитет, от друга. Теоретично това обстоятелство би могло да се обясни с късните етапи на изследване на показателите на клетъчния имунитет, когато имунокомпетентните клетки са били подложени на мощни токсични ефекти поради нарастваща функционална недостатъчност на черния дроб. Разбира се, може да се предположи, че имунната цитолиза на хепатоцитите се случва в най-ранните етапи на инфекциозния процес, вероятно дори преди появата на клинични симптоми на тежко чернодробно увреждане. Подобно предположение обаче е малко вероятно, тъй като подобни показатели на клетъчен имунитет са открити при пациенти с най-остър (светкавичен) ход на заболяването и освен това, по време на морфологично изследване на чернодробната тъкан не е открита масивна лимфоцитна инфилтрация, докато в същото време са открити непрекъснати полета на некротичен епител без явленията на резорбция и лимфоцитна агресия.
Много е трудно да се обясни морфологичната картина на острия хепатит само от гледна точка на имунната клетъчна цитолиза, следователно в ранните проучвания цитотоксичният ефект на вируса на хепатит В не е бил изключен.
В момента това предположение е частично потвърдено от откриването на вируса на хепатит B. Както показват проучванията, честотата на откриване на маркери за хепатит D е пряко зависима от тежестта на заболяването: при леки форми те се откриват при 14%, умерени - при 18%, тежки - 30% и злокачествени - при 52% от пациентите. Като се има предвид, че вирусът на хепатит D има некрозогенен цитопатичен ефект, може да се счита за установено, че коинфекцията с вируси на хепатит B и D е от голямо значение за развитието на фулминантни форми на хепатит B.
Патогенезата на хепатит В може да се представи по следния начин. След проникването на вируса на хепатит В в хепатоцитите, се предизвиква имунологична атака срещу заразените хепатоцити от Т-килъри, които отделят лимфотоксини по посока на чернодробните клетки.
Точните механизми на увреждане на хепатоцитите при хепатит B все още не са установени. Водеща роля играят активираните процеси на липидна пероксидация и лизозомни хидролази. Спусъкът може да са лимфотоксини, освобождавани от ефекторните клетки при контакта им с хепатоцитите, но е възможно самият вирус да е инициатор на процесите на пероксидация. Впоследствие патологичният процес най-вероятно се развива в следната последователност.
- Взаимодействие на фактора на агресия (лимфотоксини или вирус) с биологични макромолекули (евентуално с компоненти на мембраните на ендоплазмения ретикулум, способни да участват в процесите на детоксикация, по аналогия с други увреждащи агенти, както беше показано във връзка с тетрахлорметан).
- Образуване на свободни радикали, активиране на процесите на липидна пероксидация и повишена пропускливост на всички хепатоцелуларни мембрани (синдром на цитолизата).
- Движение на биологично активни вещества по концентрационния градиент - загуба на ензими с различна вътреклетъчна локализация, енергийни донори, калий и др. Натрупване на натрий и калций в клетките, изместване на pH към вътреклетъчна ацидоза.
- Активиране и освобождаване на лизозомни хидролази (РНКаза, ДНКаза, катепсини и др.) с разграждане на чернодробните клетки и освобождаване на автоантигени.
- Стимулиране на Т- и В-имунните системи с образуване на специфична сенсибилизация на Т-лимфоцитите към чернодробни липопротеини, както и образуване на антихепатални хуморални автоантитела.
В предложената схема на патогенезата на хепатит B, отключващият фактор са вирусните антигени, чието интензивно производство се наблюдава в най-ранните стадии на заболяването и през целия остър период, с изключение на злокачествените форми, при които производството на вирусни антигени практически спира в момента на развитие на масивна чернодробна некроза, което предопределя бързо намаляване на вирусната репликация.
Очевидно е също, че вирусните антигени активират Т- и В-системите на имунитета. По време на този процес се наблюдава характерно преразпределение на Т-лимфоцитните субпопулации, насочено към организиране на адекватен имунен отговор, елиминиране на инфектираните хепатоцити, неутрализиране на вирусните антигени, саногенеза и възстановяване.
Когато имунокомпетентните клетки взаимодействат с вирусни антигени върху хепатоцитните мембрани или по време на размножаването на вируса вътре в хепатоцита, възникват условия за активиране на процесите на липидна пероксидация, която, както е известно, контролира пропускливостта на всички клетъчни и субклетъчни мембрани.
От тази позиция, появата на цитолитичен синдром, повишена пропускливост на клетъчните мембрани, която е толкова естествена и силно характерна за вирусния хепатит, става разбираема.
Крайният резултат от синдрома на цитолизата може да бъде пълно разединяване на оксидативното фосфорилиране, изтичане на клетъчен материал и смърт на чернодробния паренхим.
Въпреки това, в по-голямата част от случаите тези процеси не придобиват такова фатално развитие. Само при злокачествени форми на заболяването патологичният процес протича лавинообразно и необратимо, тъй като се наблюдават масивна инфекция, изразен имунен процес, прекомерно активиране на процесите на пероксидация и лизозомни хидродази, както и явления на автоимунна агресия.
Същите механизми се наблюдават и при благоприятния ход на хепатит В, с единствената особеност, че всички те се реализират на качествено различно ниво. За разлика от случаите на масивна чернодробна некроза, при благоприятния ход на заболяването броят на инфектираните хепатоцити, а следователно и зоната на имунопатологична цитолиза, е по-малък, процесите на липидна пероксидация не са толкова значително засилени, активирането на киселинните хидролази води само до ограничена автолиза с незначително освобождаване на автоантигени и следователно без масивна автоагресия, т.е. всички етапи на патогенезата при благоприятния ход се осъществяват в рамките на запазената структурна организация на чернодробния паренхим и са сдържани от защитни системи (антиоксиданти, инхибитори и др.) и следователно нямат такъв разрушителен ефект.
Причините за симптомите на интоксикация при вирусен хепатит не са напълно проучени. Предложението за разграничаване между така наречената първична или вирусна интоксикация и вторична (обменна или метаболитна) може да се счита за положително, въпреки че това не разкрива интимния механизъм на възникване на общ токсичен синдром. Първо, вирусите на хепатита нямат токсични свойства, и второ, концентрацията на много метаболити не винаги корелира с тежестта на заболяването и степента на изразяване на симптомите на токсикоза. Известно е също, че концентрацията на вирусни антигени не корелира стриктно с тежестта на интоксикацията. Напротив, с увеличаване на тежестта на заболяването и следователно с увеличаване на степента на токсикоза, концентрацията на HBsAg намалява и е най-ниска при злокачествени форми по време на настъпване на дълбока чернодробна кома. В същото време честотата на откриване и титрите на специфични антивирусни антитела зависят пряко от тежестта на заболяването.
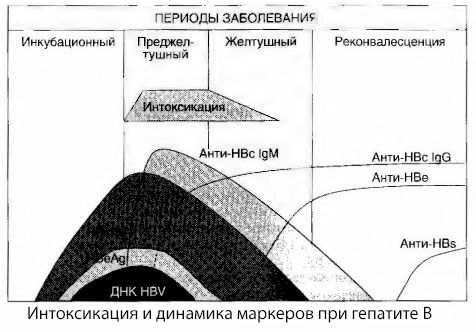
Интоксикацията се появява не в момента на регистрация на вирусни антигени, а по време на периода на циркулация в кръвта на антивирусни антитела от клас IgM към кравешкия антиген и антигена на системата Е. Освен това, при тежки и особено злокачествени форми, значителна част от пациентите дори имат анти-HBs в кръвта, което обикновено никога не се наблюдава при леки и умерени форми на заболяването.
Представените данни ни позволяват да заключим, че синдромът на токсикоза при вирусен хепатит, и по-специално хепатит B, не възниква в резултат на появата на вирусни антигени в кръвта, а е следствие от взаимодействието на вирусни антигени с антивирусни антитела от клас IgM. Резултатът от такова взаимодействие, както е известно, е образуването на имунни комплекси и евентуално на активни токсични вещества.
Симптомите на интоксикация възникват в момента на появата на имунни комплекси в свободно кръвообращение, но впоследствие такава корелация не се наблюдава.
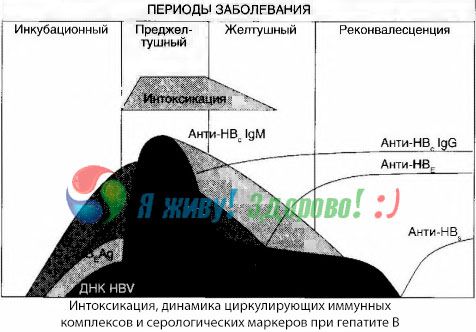
Частично обяснение за това може да се намери в изследването на състава на имунните комплекси. При пациенти с тежки форми в кръвта циркулират предимно средно големи комплекси, като в състава им, в разгара на токсичния синдром, преобладават антитела от класа, докато в периода на спад на клиничните прояви и реконвалесценция комплексите стават по-големи и в състава им започват да преобладават антитела от класа IgG.
Представените данни се отнасят до механизмите на развитие на токсичен синдром в началния период на заболяването, но при токсикоза, настъпваща в разгара на клиничните прояви, те имат само частично значение, и особено при развитието на чернодробна кома.
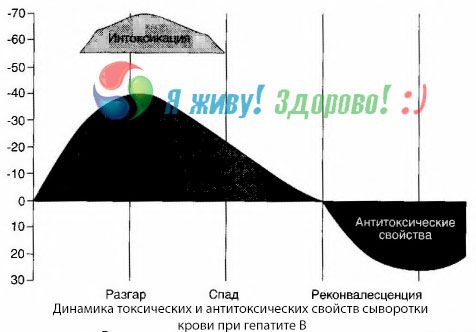
Методът на кръвните култури е показал, че при хепатит В в кръвта постоянно се натрупват токсини, освобождавани от увредената, разпадаща се чернодробна тъкан. Концентрацията на тези токсини е пропорционална на тежестта на заболяването, те са с протеинов характер.
По време на периода на възстановяване в кръвта се появяват антитела срещу този токсин; но в случай на чернодробна кома концентрацията на токсина в кръвта се увеличава рязко и антитела не се откриват в кръвта.
Патоморфология на хепатит B
Въз основа на естеството на морфологичните промени се разграничават три форми на остър хепатит В:
- циклична форма,
- масивна чернодробна некроза;
- холестатичен перихолангиолитичен хепатит.
При цикличната форма на хепатит B дистрофичните, възпалителните и пролиферативните промени са по-изразени в центъра на лобулите, докато при хепатит A те са локализирани по периферията на лобулата, разпространявайки се към центъра. Тези разлики се обясняват с различните пътища на проникване на вируса в чернодробния паренхим. Вирусът на хепатит A навлиза в черния дроб през порталната вена и се разпространява до центъра на лобулите, вирусът на хепатит B прониква през чернодробната артерия и капилярните клони, които равномерно кръвоснабдяват всички лобули, чак до техния център.
Степента на увреждане на чернодробния паренхим в повечето случаи съответства на тежестта на клиничните прояви на заболяването. При леки форми обикновено се наблюдава фокална некроза на хепатоцитите, а при умерени и тежки форми - зонална некроза (с тенденция към сливане и образуване на мостоподобна некроза при тежки форми на заболяването).
Най-големите морфологични промени в паренхима се наблюдават в пика на клиничните прояви, което обикновено съвпада с първото десетилетие на заболяването. През второто и особено третото десетилетие процесите на регенерация се засилват. Към този период некробиотичните промени почти напълно изчезват и започват да преобладават процесите на клетъчна инфилтрация с бавно последващо възстановяване на структурата на хепатоцелуларните пластинки. Пълното възстановяване на структурата и функцията на чернодробния паренхим обаче настъпва едва 3-6 месеца след началото на заболяването и не при всички пациенти.
Генерализираният характер на инфекцията при хепатит B се потвърждава от откриването на HBsAg не само в хепатоцитите, но и в бъбреците, белите дробове, далака, панкреаса, клетките на костния мозък и др.
Холестатичният (перихолангиолитичен) хепатит е специална форма на заболяването, при която най-големи морфологични промени се установяват от страна на интрахепаталните жлъчни пътища, с картина на холангиолит и перихолангиолит. При холестатичната форма холестазата протича с разширяване на жлъчните капиляри със застой на жлъчката в тях, с пролиферация на холангиоли и клетъчни инфилтрати около тях. Чернодробните клетки са засегнати незначително при тази форма на хепатит. Клинично заболяването се характеризира с продължително протичане с продължителна жълтеница. Доказано е, че причината за такъв своеобразен ход на заболяването е преобладаващият ефект на вируса върху стените на холангиола с незначителен ефект върху хепатоцитите.

