Медицински експерт на статията
Нови публикации
Глиома на мозъка
Последно прегледани: 29.06.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
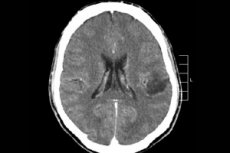
Сред многото туморни процеси на централната нервна система, най-често се диагностицира мозъчен глиом - този термин е събирателен, неоплазмата обединява всички дифузни олигодендроглиални и астроцитни огнища, астроцитом, астробластом и т.н. Такъв тумор може да има различна степен на злокачественост, образува се от глиални структури - клетки, локализирани около неврони. Основната област на локализация на глиомите са мозъчните полукълба, стените на мозъчните вентрикули и хиазмата - областта на частично пресичане на влакната на зрителния нерв. Външно туморът представлява нодуларен елемент с розов или червеникав оттенък, кръгла или вретеновидна конфигурация с неясни граници. [ 1 ]
Епидемиология
В около 5% от случаите глиомите са свързани с наследствени патологии - по-специално неврофиброматоза и други синдроми с доминантно унаследяване. Експертите посочват, че абсолютното мнозинство от мозъчните глиоми се развиват спорадично - тоест без ясна причина.
Като цяло, първичните неоплазми на централната нервна система представляват приблизително 2% от всички тумори, или малко над 21 случая на сто хиляди души от населението. Сред тях глиомите се срещат в 35-36% от случаите, а повече от 15% от тях са глиобластоми.
Според някои данни, глиомът засяга мъжете по-често от жените - туморът е особено често срещан сред хора над 50 години.
Глобалната честота на глиоми сред възрастните хора се е увеличила значително през последните десетилетия. Причините за това явление все още не са установени.
Според дефиницията на Световната здравна организация са идентифицирани три основни варианта на глиални тумори, различаващи се по своите хистологични характеристики. Това са олигодендроглиоми, астроцитоми и комбинирани олигоастроцитоми. Честотата на всеки подтип на нискозлокачествена патология не е надеждно определена. Някои проучвания показват увеличение на честотата на олигодендроглиомите от 5% до 30% и намаляване на честотата на астроцитомите.
Глиалните тумори са способни да инфилтрират мозъчната тъкан и по-голямата част от нискостепенните огнища стават злокачествени в рамките на няколко години. [ 2 ]
Причини мозъчни глиоми
Мозъчният глиом е цяла група туморни процеси, чиято обща черта е образуването им от глиални структури на ЦНС, разположени в мозъчната тъкан. Такива тумори се разделят на два хистопатологични варианта: високо злокачествени и ниско злокачествени глиоми.
Източникът на образуване на растеж са невроглиалните клетки (астроцити, олигодендроцити), които осигуряват структурната основа и жизнеспособността на мозъчните неврони.
Глиалните туморни процеси се различават значително по структура, мутационни промени в гените, агресивност, клинични характеристики, диагностични характеристики, отговор на лечението и прогноза на пациентите. Ембрионалните и епендималните неоплазми на централната нервна система - по-специално медулобластомите и епендимомите - се различават по хистологичната си структура, но са сходни по отношение на лечението.
Глиалните елементи са класифицирани за първи път като отделна структурна категория на нервната система в края на 19 век.
Невроглиалната тъкан се състои от клетки, които имат спомагателни функции: трофична, опорна, защитна, секреторна. Невроните и глиоцитите съществуват заедно помежду си, те заедно образуват нервната система и имат голямо значение в общите процеси на жизнената дейност на организма.
Глиоцитите се категоризират грубо в няколко основни форми: астроцити, олигодендроцити, епендимални клетки и микроглия.
Към днешна дата учените не могат да отговорят на въпроса за достоверните причини за образуването на невроглиални тумори. Предполага се, че известен отрицателен принос имат радиоактивните ефекти, инфекциозните заболявания, интоксикациите (особено химическите, професионалните). Наследственият фактор също е важен.
Мозъчните глиоми възникват от анормални невроглиоцити, които имат генетичен дефект, водещ до анормален растеж и функционалност - такива структури се наричат „незрели“. Непълните клетки по-често се намират в една област, където се образува туморът.
Казано по-просто, образуването на глиални клетки е резултат от хаотичен и спорадичен растеж на модифицирани невроглиални клетки. Процесът може да се развие от епендимоцити, олигодендроцити, астроцити (астроцитом, включително гигантоклетъчен и анапластичен). [ 3 ]
Рискови фактори
Въпреки факта, че експертите не могат точно да характеризират причините за образуването на глиални онкопатологии, в някои случаи появата им може да бъде предотвратена чрез елиминиране на основните рискови фактори:
- Йонизиращото лъчение има канцерогенна активност, може да причини развитие на левкемия и образуване на ракови процеси с плътна структура, включително при хора в млада възраст. Честите и неразумни радиологични медицински процедури, ултравиолетовото облъчване (включително солариум) също принадлежат към потенциални канцерогенни ефекти и могат да причинят появата на тумори в различни органи, включително мозъка.
- Професионалните неблагоприятни ефекти, интоксикациите, често имат причинно-следствена връзка с развитието на ракови тумори. Производството на каучук и стъкло, пестициди и горива, метали и текстил, бои и лабораторни реактиви се считат за особено опасни. В риск са работниците в аерокосмическата, въгледобивната и металургичната промишленост, химическите и страничните производствени предприятия, строителните материали и електродите, горивата и смазочните материали, пластмасите и мономерите.
- Замърсяването на въздуха, водата и почвата е причина за до 4% от всички ракови патологии в света. Канцерогените, присъстващи в големи количества в околната среда, попадат в тялото с вдишвания въздух, питейната вода и храната. Животът в екологично опасни райони - в близост до големи промишлени съоръжения, натоварени транспортни възли - се счита за особено опасен.
- Инфекциозните патологии - по-специално вирусните инфекции - също могат да създадат благоприятни условия за развитието на тумори. Важно е да се има това предвид и да се ваксинирате предварително, както и да се предотвратят инфекциозни и паразитни заболявания.
- Тютюневата и алкохолната интоксикация се считат за рискови фактори за много видове рак, не само за мозъчни глиоми.
- Недостатъчна физическа активност, наднормено тегло, неправилно хранене, метаболитни нарушения, травми на главата, съдови патологии - допълнителни стресови фактори, които могат да провокират началото на вътреклетъчни нарушения.
- По-напредналата възраст е най-честият период за развитие на неоплазми в тялото, така че тези над 55 години трябва да се грижат особено за собственото си здраве.
Основният и най-значим рисков фактор за развитието на глиом обаче остава наследствената предразположеност.
Патогенеза
Към днешна дата експертите имат редица предположения относно развитието на мозъчни глиоми. Всяка теория има свои собствени основания, но единственият правилен и надежден патогенетичен механизъм учените все още не са идентифицирали. В повечето случаи говорим за следните фактори за развитието на неоплазми:
Неуспех на ембриогенезата, който се състои в нарушаване на полагането на органи и образуването на „грешни“ клетъчни структури;
- Излагане на йонизиращи лъчи, потенциални канцерогени под формата на химични агенти, хранителни добавки и др.;
- Травма на главата;
- Генни нарушения, предавани от поколение на поколение („фамилен“ глиом);
- Имунна дисфункция, невроинфекции.
Повечето глиоми имат дифузен растеж, с проникване в околната нормална мозъчна тъкан. В зависимост от степента на злокачественост, туморът може да се развива в продължение на няколко години без никаква проява. При агресивен ход, симптоматиката бързо се увеличава в продължение на няколко месеца.
Част от туморогенезата се дължи на дизембриогенетични промени.
Мозъчният ствол може да бъде засегнат на различни нива: дифузният глиом на мозъчния ствол, от своя страна, ще се различава както анатомо-морфологично, така и клинично. Някои такива неоплазми - по-специално глиомът на квадриплегичната пластина - могат да бъдат относително доброкачествени, без признаци на прогресия. Глиомът на моста, от друга страна, се характеризира със своята специфична злокачественост, агресивност и лоша прогноза.
Дифузните лезии на мозъчните структури, при които в патологичния процес са въвлечени повече от три анатомични зони на големите полукълба, с възможна перивентрикуларна дивергенция и преминаване през корпуса, се наричат глиоматоза. [ 4 ]
Наследствен ли е мозъчният глиом?
Добре доказан риск от образуване на мозъчен глиом е наследственият - тоест наличието на подобни или други интрацеребрални тумори при преки предци или в същото поколение. Радиоактивното облъчване и редовният или продължителен контакт с потенциални канцерогени изострят ситуацията.
Не само глиомите могат да бъдат наследени, но и заболявания, които са съпроводени с повишен туморен растеж, без да се има предвид локализацията - по-специално, това може да бъде неврофиброматоза тип 1 и 2, синдром на Ли-Фраумени, Хипел-Линдау. Често в глиомните клетки се откриват промени в определени гени или хромозоми.
Основните патологии, свързани с развитието на глиом при хората, са обобщени в таблицата:
Патология |
Хромозома |
Джийн |
Разнообразие от неоплазми |
Синдром на Ли-Фраумени |
17р13 |
TR53 |
Невроектодермални неоплазми, астроцитом. |
Неврофиброматоза |
17q11 |
НФ1 |
Глиом на зрителния нерв, пилоцитен астроцитом, неврофиброматоза |
Синдром на Тюркот |
3p21, 7p22 |
HMLH1, HPSM2 |
Астроцитом |
Туберозна склероза (синдром на Бърневил). |
9q34, 16p13 |
TSC1, TSC2 |
Гигантоцелуларен субепендимален астроцитом |
Независимо от естеството на глиалния тумор, дали е спорадичен случай или наследствена патология, той е нарушение с експресията на патологично променен ген. Освен неоплазмите, образувани в резултат на ефектите на обучението, в други ситуации причините за генетичните промени остават неясни.
Симптоми мозъчни глиоми
Характеристиките на фокалната симптоматика зависят пряко от областта на локализация на мозъчния глиом и стават следствие от всякакви ендокринни нарушения, компресия на нервната тъкан или локални деструктивни процеси.
Ако неоплазмата се намира в париеталната зона, тогава човек е доминиран от такива прояви като гърчове, сензорни нарушения, увреждане на слуха.
Когато глиомът е локализиран в областта на доминантното полукълбо, се откриват нарушения на говора, аграфия, агнозия.
Неоплазмите на темпоралния лоб често са съпроводени с конвулсивни припадъци, афазия, нарушено обоняние и зрителна функция, както и диспнея.
Когато вътречерепното налягане се повиши, се развива съответна картина с ограничаване на зрителните полета, парализа на очните мускули и хемиплегия.
Поради специфичността на туморния процес, мозъчният глиом винаги е съпроводен от неврологични симптоми в по-голяма или по-малка степен. В началото се наблюдава забележима обща слабост, пациентът постоянно иска да спи, работоспособността е нарушена, мисловните процеси са забавени. Именно на този етап съществува висок риск от поставяне на неправилна диагноза и в резултат на това предписване на неправилно лечение. Сред другите неспецифични прояви са:
- Вестибуларни нарушения, включително нестабилна походка, загуба на равновесие (напр. при каране на велосипед или изкачване на стълби), изтръпване на крайниците и др.;
- Постепенно влошаване на зрението, удвояване на зрителната картина;
- Влошаване на слуховата функция;
- Неясна реч;
- Гадене и повръщане под формата на пристъпи, независими от храна или напитки;
- Отслабване на мимическите мускули и други лицеви мускули;
- Дискомфорт при преглъщане;
- Редовни главоболия (често сутрин).
Клиничната картина постепенно се разширява и влошава: при някои пациенти това се случва бавно, при други - рязко, буквално „пред очите им“, в рамките на няколко седмици. В последния случай говорим за агресивен, бързо развиващ се глиом на мозъка.
Първи признаци
Глиомът на мозъка в ранните етапи на развитие няма изразена симптоматика. Първите прояви често се бъркат с признаци на други, по-малко опасни патологии.
Като цяло, клиничната картина на глиома е разнообразна и се определя от местоположението и размера на патологичния фокус. С нарастването на неоплазмата се развиват и засилват общи мозъчни симптоми:
- Упорита и редовна главоболие, която не се повлиява от стандартни лекарства (нестероидни противовъзпалителни средства);
- Периодично гадене, понякога до степен на повръщане;
- Неприятно, тежко усещане в областта на очната ябълка;
- Припадъци.
Церебралните прояви са особено интензивни, когато туморът прораства в камерите или ликворната система. Оттичането на цереброспиналната течност е нарушено, вътречерепното налягане се повишава и се развива хидроцефалия. Процесът засяга определена част от мозъка, което влияе върху развитието на съответната клиника:
- Има проблеми със зрителната функция;
- Нарушена реч;
- Появяват се вестибуларни нарушения (замаяност, нарушена координация на движенията);
- Пареза, парализа на ръцете, краката;
- Паметта и концентрацията са нарушени;
- Мисловните процеси са нарушени;
- Появяват се поведенчески разстройства.
В началния етап симптомите практически липсват или са толкова незначителни, че не привличат внимание. Поради тази причина експертите силно препоръчват редовни профилактични прегледи и контролни прегледи. В крайна сметка, колкото по-рано се открие туморният процес, толкова по-големи са шансовете за излекуване и оцеляване. [ 5 ]
Глиом на мозъка при дете
Сред многото мозъчни тумори, открити в детска възраст, процентът на глиомите варира от 15 до 25%. Децата могат да се разболеят в ранните си юношески и ранните си двадесет години, въпреки че е много рядко бебета под 3-годишна възраст да се разболеят.
Патологията започва на фона на мутация на глиални клетки. Към днешна дата няма отговор на въпроса защо се случва тази мутация.
Единственото нещо, което е надеждно научено, е, че някои наследствени заболявания, свързани с повишен риск от растеж на тумора, също увеличават вероятността от развитие на мозъчен глиом.
Освен това, учените са открили, че глиалните клетки могат да имат различия в отделни гени или хромозоми. Поради това разстройство се задейства мутационен механизъм, който не е наследствен. Възможно е това да се случи в един от най-ранните етапи на развитие.
Доказан факт е, че наличието на остра левкемия или ретинобластом в анамнезата на детето, или облъчване на мозъка по каквато и да е друга причина, значително увеличава рисковете от образуване на глиом (след определен период от време).
Симптоматологията в детска възраст зависи от степента на злокачественост и локализацията на патологичния фокус. Разграничават се специфични и неспецифични симптоми:
- Неспецифичните симптоми не са „обвързани“ с областта, където се намира глиомът. Честите прояви могат да включват главоболие, световъртеж, лош апетит, повръщане без връзка с приема на храна, загуба на тегло (по неизвестни причини), постоянно чувство на умора, спад в академичните постижения, затруднена концентрация, поведенчески нарушения. Тези признаци се дължат на компресия на вътречерепните структури, което може да се обясни като директен натиск от нарастващата маса, и нарушение в циркулацията на цереброспиналната течност. Съществува риск от мозъчно хидроцеле.
- Специфичната симптоматика зависи от непосредственото местоположение на глиалния патологичен фокус. Например, туморът на малкия мозък обикновено е съпроводен с нарушена походка и равновесие при децата. Лезията на големия мозък се проявява с конвулсивни припадъци, а растежът на тумора в гръбначния мозък - парализа на мускулатурата. Случва се зрението на бебето да се влоши рязко, съзнанието да се наруши, сънят да се наруши или да възникне някакъв друг проблем в развитието.
Като правило, в детска възраст злокачественият глиом се проявява след няколко седмици или месеци от развитието си: често се характеризира с бърз и неконтролиран растеж на неоплазмата.
Децата със злокачествени глиални тумори се лекуват от лекари в педиатрични клинични центрове, специализирани в детска онкология. Като правило се използва хирургично лечение, лъчетерапия и химиотерапия.
Най-важната стъпка в лечението е неврохирургията. Колкото по-радикална е тя, толкова по-големи са шансовете на детето за излекуване. Но хирургическата интервенция не винаги е възможна: по-специално, проблеми могат да възникнат при отстраняването на глиоми на мозъчния ствол, както и при лъчетерапия при деца под 3-годишна възраст.
Глиомите на централния мозък (междинен и среден мозък) са трудни за пълно отстраняване, тъй като съществува риск от увреждане на здрава тъкан. Ако пълната резекция на тумора е невъзможна, на пациента се предписва палиативно лечение.
Децата със злокачествени глиоми се лекуват съгласно стандартизирани протоколи, определени чрез строго контролирани клинични изпитвания. Най-често срещаните протоколи са следните:
- HIT HGG 2007: включва лечение на деца на възраст 3-17 години.
- HIT SKK: подходящ за кърмачета (до тригодишна възраст) и не включва лъчетерапия.
Статистиката за педиатричната преживяемост при глиоми като цяло не е много оптимистична. Въпреки това, в никакъв случай не е възможно да се предвиди предварително ефективността на лечебните мерки за конкретно дете. Важно е стриктно да се спазват всички предписания на лекаря, което значително увеличава шансовете за възстановяване.
Форми
Глиомите могат да бъдат нискозлокачествени и високозлокачествени, с интензивен растеж и склонност към метастазиране. Важно е да се разбере, че нискозлокачествеността не е синоним на безопасност на тумора. Всяка мозъчна неоплазма създава допълнителен обем, притиска мозъчните структури, което води до тяхното изместване и повишено вътречерепно налягане. В резултат на това пациентът може да почине.
Съществуват два основни вида злокачествени астроцитоми. Това са глиобластоми и анапластични астроцитоми, които се подразделят според молекулярните промени. Вторичните злокачествени тумори, които са се развили от астроцитоми и имат ниска степен на злокачественост, се срещат най-често при млади пациенти. Първоначално злокачествените тумори от глиален тип се срещат по-често при пациенти в напреднала възраст.
В зависимост от структурното местоположение, глиомите се разделят на:
- Супратенториален (с локализация над малкия мозък в областта на страничните вентрикули, големите полукълба);
- Субтенториален (с локализация под малкия мозък в задната черепна ямка).
Според хистологичните характеристики се разграничават следните видове глиоми:
- Астроцитният глиом е най-често срещаният. От своя страна той се подразделя на нодуларен и дифузен (последният може да се характеризира с бърз растеж и инсултна форма).
- Олигодендроглиом - среща се при 5% от пациентите. Има петрификати - области на калцификация, най-често във фронталния лоб.
- Епендимален глиом - расте от структурите, покриващи стените на централния канал на гръбначния мозък и вентрикулите. Често расте в дебелината на мозъчното вещество, както и в лумена на мозъка.
Възможни са и смесени патологични огнища като субепендимом, олигоастроцитом и др.
Всички глиоми се категоризират в следните етапи:
- Бавнорастящи относително доброкачествени неоплазми без явни клинични симптоми.
- Бавнорастящи „гранични“ глиоми, които постепенно се трансформират в стадий III и по-нататък.
- Злокачествен глиом.
- Злокачествен глиом с интензивен агресивен растеж и разпространение, с лоша прогноза.
Колкото по-нисък е стадият на злокачествено заболяване, толкова по-малка е вероятността от метастази и рецидив на отстранената неоплазма и толкова по-големи са шансовете за излекуване на пациента. Най-голяма опасност представлява мултиформеният глиобластом, нискодиференциран процес с интензивен растеж и развитие. [ 6 ]
Възможни и най-често срещани варианти на невроглиом:
- Глиомът с лезии на мозъчния ствол и моста се намира в областта, където мозъкът се свързва с гръбначния мозък. Именно там се локализират важни невроцентрове, отговорни за дихателната, сърдечната и двигателната функция. Ако тази зона е увредена, работата на вестибуларния и говорния апарат се нарушава. Често се открива в детска възраст.
- Зрителният глиом засяга невроглиалните клетки, които обграждат зрителния нерв. Патологията причинява зрително увреждане и екзофталм. Развива се по-често при деца.
- Ниският злокачествен невроглиом се характеризира с бавен растеж, локализиран по-често в големите полукълба и малкия мозък. Среща се по-често при млади хора (юноши и млади хора около 20-годишна възраст).
- Глиомът на corpus callosum е по-характерен за лица между 40 и 60-годишна възраст и най-често се представя от глиобластом.
- Глиомът на хиазмата е локализиран в зоната на зрителния преход, така че е съпроводен с миопия, загуба на зрително поле, оклузивна хидроцефалия и невроендокринни нарушения. Може да се появи във всяка възраст, но най-често засяга пациенти с неврофиброматоза тип I.
Усложнения и последствия
Глиоми с ниска степен на злокачественост (степен I-II, силно злокачествени - напр. астроцитом, олигоастроцитом, олигодендроглиом, плеоморфен ксантоастроцитом и др.) и висока степен на злокачественост (степен III-IV - глиобластом, анапластичен олигодендроглиом, олигоастроцитом и астроцитом). Глиомите от степен IV са особено злокачествени.
Глиомът на мозъчния ствол има много неблагоприятна прогноза именно защото неоплазмата засяга такъв мозъчен регион, където са концентрирани най-важните нервни връзки между мозъка и крайниците. Дори сравнително малък тумор в тази област е достатъчен, за да влоши бързо състоянието на пациента и да провокира парализа.
Не по-малко неблагоприятни последици възникват, когато са засегнати и други мозъчни области. Често става въпрос за тумор на мозъчната кора, който не дава шанс за дълга продължителност на живота на пациента, въпреки лечението. Често е възможно само да се отложи смъртта.
Според медицинската статистика петгодишната преживяемост често е само 10-20%. Въпреки че тези цифри до голяма степен зависят както от степента на злокачественост, така и от точната локализация и обем на извършената хирургична интервенция. След пълно отстраняване на патологичния фокус, преживяемостта се увеличава значително (понякога до 50%). Липсата на лечение или невъзможността му (по една или друга причина) гарантирано води до смърт на пациента.
По-голямата част от нискозлокачествените глиални тумори са способни да инфилтрират мозъчната тъкан и да се малигнизират в продължение на няколко години.
Рискът от рецидив на глиома се счита от експертите за „много вероятен“. Въпреки това лечението не бива да се пренебрегва: важно е да се осигури добро качество на живот възможно най-дълго.
Рецидивиращите глиоми винаги имат по-лоша прогноза от първичните тумори. Въпреки това, съвременните протоколи за лечение, базирани на проучвания за терапевтична оптимизация, често постигат достатъчно добри резултати при пациенти дори с високо злокачествени неоплазми.
Възможни резултати след химиотерапия:
- Измършавяване, измършавяване, храносмилателни нарушения, заболявания на устната кухина;
- Повишена възбудимост на централната нервна система, астения;
- Влошаване на слуховата функция, шум в ушите и звънене;
- Припадъци, депресивни разстройства;
- Хипертонична криза, промяна в кръвната картина;
- Бъбречна недостатъчност;
- Алергични процеси, косопад, поява на пигментни петна по тялото.
След химиотерапия пациентите отбелязват изразено отслабване на имунната система, което може да причини развитието на различни инфекциозни патологии.
Диагностика мозъчни глиоми
Глиом на мозъка може да се подозира по следните признаци:
- Пациентът има локализирани или генерализирани гърчове, които са характерни за кортикалната локализация на неоплазмата и бавното ѝ развитие. Епи-гърчове се откриват при 80% от пациентите с нискостепенни глиални тумори и при 30% от пациентите с високостепенни глиоми.
- Повишеното вътречерепно налягане е особено характерно за маси, разположени в десния фронтален и париетален лоб. Свързаното с високо вътречерепно налягане нарушение на кръвообращението и ликворообращението води до появата на постоянна и нарастваща главоболие, гадене с повръщане, зрителни нарушения, сънливост. Наблюдава се оток на зрителния нерв, парализа на отклоняващия нерв. Повишаването на вътречерепното налягане до критични стойности може да доведе до развитие на кома и смърт. Друга причина за високо вътречерепно налягане е хидроцефалията.
- Пациентът има нарастваща фокална картина. В супратенториалните формации се нарушават двигателната и сензорната сфера, прогресират хемиопия, афазия и когнитивни нарушения.
Ако лекарят подозира наличието на мозъчно новообразувание, оптимално е да се извърши ЯМР без или с въвеждане на контрастно вещество (гадолиний), за да се установи неговото местоположение, размер и допълнителни характеристики. Ако магнитно-резонансната томография не е възможна, се извършва компютърна томография, а като метод за диференциация се използва магнитно-резонансна спектроскопия. Въпреки информативността на тези диагностични методи, окончателната диагноза се поставя само след хистологично потвърждение по време на резекция на туморното огнище.
Предвид горепосочените критерии, се препоръчва диагнозата да започне с обстойно снемане на анамнеза, оценка на сомато-неврологичния статус и функционалното състояние. Неврологичният статус се оценява заедно с определянето на вероятни интелектуални и мнестични разстройства.
Препоръчителни лабораторни изследвания:
- Пълноценен общ клиничен кръвен анализ;
- Пълен кръвен биохимичен тест;
- Анализ на урината;
- Изследване на коагулацията на кръвта;
- Анализ за онкологични маркери (AFP, бета-hCG, LDH - от значение при съмнение за лезия на епифизната зона).
За изясняване на прогностичните точки при пациенти с глиобластом и анапластичен астроцитом се оценяват мутацията в гена IDH1|2-1 и метилирането на гена MGMT. При пациенти с олигодендроглиом и олигоастроцитом се определя коделация 1p|19q.
Инструменталната диагностика, на първо място, е представена от задължителното магнитно-резонансно изображение на мозъка (понякога - и гръбначния мозък). ЯМР се извършва в три проекции, използвайки стандартни режими T1-2, FLAIR, T1 с контраст.
При показания се извършват ултразвуково изследване на съдовата мрежа, функционално магнитно-резонансно изследване на двигателния и говорния отдел, както и ангиография, спектроскопия, MR трактография и перфузия.
Допълнителните изследвания могат да включват:
- Електроенцефалография на мозъка;
- Консултации с неврохирург, онколог, рентгенолог, офталмолог, рентгенолог.
Диференциална диагноза
Диференциалната диагноза задължително се провежда с нетуморни патологии - по-специално с кръвоизлив, причинен от артериовенозна или артериална малформация, както и с псевдотуморни демиелинизиращи процеси, възпалителни заболявания (токсоплазмоза, мозъчен абсцес и др.).
Освен това, разграничете първичния туморен фокус и метастазите в централната нервна система.
Със съвременните възможности на магнитно-резонансната томография е възможно да се извършват диагностични мерки достатъчно точно, за да се установи произходът на първичния фокус в ЦНС. ЯМР на мозъка се извършва със или без контраст, в T1, T2 FLAIR режим - в три проекции, или тънки срезове в аксиална проекция (SPGR режим). Тези диагностични методи позволяват точно да се определи местоположението, размерът, структурните характеристики на неоплазмата, връзката ѝ със съдовата мрежа и близките мозъчни области.
Освен това, като част от диференциалната диагноза може да се извърши компютърна томография (КТ) (със или без контраст), КТ ангиография (ЯМР ангиография), ЯМР трактография, ЯМР или КТ перфузия. КТ/ПЕТ на мозъка с метионин, холин, тирозин и други аминокиселини се използва, когато е показано.
Лечение мозъчни глиоми
Специфичната терапия се състои от хирургични, химиотерапевтични и лъчетерапия. Задължително е, ако е възможно, да се извърши пълна резекция на туморното огнище, което позволява бързо облекчаване на симптомите и хистологично потвърждаване на диагнозата.
Облъчването има положителен ефект върху увеличаването на продължителността на живота на пациентите. Стандартно се прилага обща доза от 58 до 60 Gy, разделена на индивидуални дози облъчване от 1,8-2 Gy. Туморът се облъчва локално, като допълнително се обхвават до 3 см около него. Лъчетерапията е по-приемлива за разлика от брахитерапията. В някои случаи се препоръчват радиохирургични методи, които се състоят в облъчване с гама-нож или линеен газов педал, както и неутронно-улавяща борна терапия.
Необходимостта от адювантна химиотерапия е спорна. В някои случаи препаратите с нитрозоурея позволиха да увеличат продължителността на живота на пациентите до година и половина, но някои резултати от използването на такива химиопрепарати бяха отрицателни. Днес активно се използват цитотоксични средства, неоадювантна терапия (преди лъчетерапия), комбинирани лекарства, интраартериална химиотерапия или химиотерапия с високи дози с последваща трансплантация на стволови клетки.
Като цяло, за успешното лечение на глиомите е много важен комплексният подход, чийто обхват зависи от местоположението и степента на злокачественост на масата, нейния размер и общото здравословно състояние на пациента.
По отношение на глиома на мозъчния ствол, хирургичната интервенция се използва рядко. Основното противопоказание за операцията е зоната на локализация на фокуса - в непосредствена близост до жизненоважни части. В някои случаи е възможно отстраняването на глиома на ствола с помощта на микрохирургични методи, с предоперативна и следоперативна химиотерапия. Такава интервенция е много сложна и изисква специална квалификация на неврохирург.
Лъчехирургията и по-специално стереотактичната хирургия с облъчване с високи йонизиращи дози е доста ефективна. Използването на такава техника в ранните етапи на развитие на неоплазмата понякога позволява постигане на продължителна ремисия или дори пълно излекуване на пациента.
Лъчетерапията често се комбинира с химиотерапия, което подобрява ефикасността на интервенциите и намалява радиационното натоварване. При глиоми не всички химиопрофилактични средства са терапевтично успешни, така че те се предписват индивидуално и рецептите се коригират, ако е необходимо.
За намаляване на болката и понижаване на вътречерепното налягане, независимо от основното лечение, се предписва симптоматична терапия - по-специално кортикостероидни лекарства, аналгетици, успокоителни.
Лекарства
Кортикостероидните лекарства повлияват отока, намаляват тежестта на неврологичните симптоми в продължение на няколко дни. Въпреки това, поради множество странични ефекти и повишена вероятност от нежелани взаимодействия с химиотерапевтичните лекарства, се използват минимално ефективни дози стероиди, като приема им се прекратява възможно най-скоро (напр. след операция).
Антиконвулсантите се използват систематично като вторична превантивна мярка при пациенти, които вече са преживели епилептични припадъци. Тези лекарства могат да причинят сериозни нежелани симптоми и също така да взаимодействат с химиотерапевтичните лекарства.
Антикоагулантите са особено важни в следоперативния етап, тъй като рисковете от образуване на тромбофлебит при глиом са доста високи (до 25%).
Очаква се добър ефект от приема на антидепресанти-анксиолитици. Употребата на метилфенидат 10-30 mg/дневно в два приема често позволява оптимизиране на когнитивните способности, подобряване на качеството на живот, поддържане на работоспособността.
Неврологичната недостатъчност и признаците на мозъчен оток (главоболие, нарушения на съзнанието) се елиминират чрез кортикостероидни лекарства - по-специално преднизолон или дексаметазон. |
Схемата и дозировката на кортикостероидите се избират индивидуално, като се прилага минималната ефективна доза. В края на курса на лечение лекарствата се спират постепенно. |
Кортикостероидите се приемат заедно с гастропротективни лекарства - блокери на протонната помпа или H2-хистаминови блокери. |
Диуретиците (Фуроземид, Манитол) се предписват при силно подуване и изместване на мозъчните структури, като допълнение към кортикостероидните лекарства. |
В случай на конвулсивни припадъци (включително анамнеза) или епилептиформни симптоми на електроенцефалограма, допълнително се предписва антиконвулсивна терапия. Антиконвулсантите не се предписват с профилактична цел. |
На пациенти с индикации за химиотерапия се препоръчва прием на антиконвулсанти, които не повлияват функцията на чернодробните ензими. Лекарства по избор: Ламотрижин, Валпроева киселина, Леветирацетам. Не трябва да се използват: Карбамазепин, Фенобарбитал. |
Главоболието при мозъчни глиоми се лекува с кортикостероидно лечение. |
В някои случаи на главоболие могат да се използват нестероидни противовъзпалителни средства или трамадол. |
Ако пациентът приема нестероидни противовъзпалителни лекарства, те се спират няколко дни преди операцията, за да се сведе до минимум вероятността от кървене по време на операцията. |
В определени случаи на болка могат да се препоръчат наркотични аналгетици - като фентанил или тримеперидин. |
За предотвратяване на белодробна емболия от третия следоперативен ден се предписва приложение на нискомолекулни хепарини - по-специално, еноксапарин натрий или надропарин калций. |
Ако пациентът е на системно антикоагулантно или антиагрегантно лечение, той се прехвърля на нискомолекулни хепарини не по-късно от седмица преди хирургичната интервенция, с по-нататъшното им спиране ден преди операцията и възобновяване 24-48 часа след операцията. |
Ако пациент с глиом има венозна тромбоза на долните крайници, се провежда лечение с директни антикоагуланти. Не се изключва възможността за поставяне на CAVA-филтър. |
Химиотерапия за злокачествени глиоми на мозъка
Основните режими на противотуморна химиотерапия за глиоми се считат за:
- Ломустин 100 mg/m² на първия ден, винкристин 1,5 mg/m² на първия и осмия ден, прокарбазин 70 mg/m² от осмия до двадесет и първи ден, курсове на всеки шест седмици.
- Ломустин 110 mg/m² на всеки шест седмици.
- Темозоломид 5/23 150 до 200 mg/m² от първия до петия ден, на всеки 28 дни.
- Темозоломид като част от химиолъчева терапия, 75 mg/m² всеки ден, през който се прилага лъчетерапия.
- Темозоломид с цисплатин или карбоплатин (80 mg/m²) и Темозоломид 150-200 mg/m² от 1-ви до 5-ти ден на всеки 4 седмици.
- Темозоломид 7/7 в доза 100 mg/m² на 1-ви до 8-ми и 15-22-ри ден от курса, с повторение на всеки четири седмици.
- Бевацизумаб 5 до 10 mg/kg на първия и петнадесетия ден и Иринотекан 200 mg/m² на първия и петнадесетия ден, повтаряно на всеки четири седмици.
- Бевацизумаб 5 до 10 mg/kg на първия, петнадесетия и двадесет и деветия ден и Ломустин 90 mg/m² на първия ден на всеки шест седмици.
- Бевацизумаб 5 до 10 mg/kg на първия и петнадесетия ден, Ломустин 40 mg на първия, осмия, петнадесетия и двадесет и втория ден, повтаряно на всеки шест седмици.
- Бевацизумаб 5 до 10 mg/kg на първия и петнадесетия ден, повтаряно на всеки четири седмици.
Цитостатичните лекарства в много случаи успешно инхибират растежа на туморните клетки, но не показват селективност към здрави тъкани и органи. Поради това експертите са идентифицирали редица противопоказания, при които химиотерапията на глиома е невъзможна:
- Прекомерна индивидуална чувствителност към химиопрофилактични средства;
- Декомпенсация на сърдечната, бъбречната, чернодробната функция;
- Депресирана хематопоеза в костния мозък;
- Проблеми с надбъбречната функция.
Химиотерапията се прилага с изключително внимание:
- Пациенти със значителни нарушения на сърдечния ритъм;
- С диабет;
- При остри вирусни инфекции;
- При пациенти в напреднала възраст;
- Пациенти, страдащи от хроничен алкохолизъм (хронична алкохолна интоксикация).
Най-сериозният страничен ефект на химиопрофилактичните лекарства е тяхната токсичност: цитостатиците селективно пречат на функционалността на кръвните клетки и променят състава им. В резултат на това намалява масата на тромбоцитите и еритроцитите и се развива анемия.
Преди да предпише на пациента курс химиотерапия, лекарят винаги взема предвид степента на токсичност на лекарствата и вероятните усложнения след тяхното приложение. Курсовете на химиотерапия винаги се наблюдават внимателно от специалисти и се извършва редовен кръвен контрол.
Възможни последици от цитостатичната терапия:
- Измършавяване, измършавяване;
- Затруднено преглъщане на храна, сухи лигавици, пародонтит, диспепсия;
- Нестабилност на централната нервна система, маниакално-депресивни разстройства, гърчов синдром, астения;
- Влошаване на слуховата функция;
- Повишаване на кръвното налягане до развитие на хипертонична криза;
- Намаляване на тромбоцитите, червените кръвни клетки, белите кръвни клетки, множество кръвоизливи, вътрешни и външни кръвоизливи;
- Бъбречна недостатъчност;
- Алергични процеси;
- Косопад, поява на области с повишена пигментация.
След курсове на химиотерапия, пациентите имат повишен риск от развитие на инфекциозни заболявания, а мускулните и ставните болки са често срещани.
За да се намали рискът от нежелани постхимиотерапевтични ефекти, задължително се предписват допълнителни рехабилитационни мерки, чиято цел е възстановяване на нормалната кръвна картина, стабилизиране на сърдечно-съдовата дейност, нормализиране на неврологичния статус. Задължително се практикува достатъчна психологическа подкрепа.
Хирургично лечение
Операцията се извършва, за да се отстрани максимално туморният фокус, което от своя страна би трябвало да намали вътречерепното налягане, да намали неврологичната недостатъчност и да осигури необходимия биоматериал за изследване.
- Операцията се извършва в специализирано неврохирургично отделение или клиника, чиито специалисти имат опит в невро-онкологични интервенции.
- Хирургът извършва достъп чрез пластична костна трепанация в областта на предполагаема локализация на глиома.
- Ако неоплазмата е разположена анатомично близо до двигателни области или пътища, или в ядрата, или по протежение на черепномозъчни нерви, се използва интраоперативно неврофизиологично наблюдение.
- Невронавигационни системи, интраоперативна флуоресцентна навигация с 5-аминолевуленова киселина е желателна за максимално отстраняване на неоплазмата.
- След интервенцията се извършва контролна компютърна томография или ядрено-магнитен резонанс (със или без инжектиране на контраст) на 1-2 ден.
Ако хирургичната резекция на глиома е невъзможна или първоначално е призната за нецелесъобразна, или ако се подозира лимфом на централната нервна система, се извършва биопсия (отворена, стереотактична, с навигационен мониторинг и др.). |
Пациентите с церебрална глиоматоза се потвърждават чрез стереотактична биопсия, тъй като терапевтичната тактика до голяма степен зависи от хистологичната картина. |
В определени ситуации - при пациенти в напреднала възраст, при тежки неврологични нарушения, при локализация на глиом в торса и други жизненоважни части - лечението се планира въз основа на симптомите и образната информация след обща медицинска консултация. |
На пациенти с пилоиден астроцитом, както и с нодуларни форми на неоплазми на мозъчния ствол и екзофитни процеси, се препоръчва резекция или отворена биопсия. |
Пациенти с дифузен понтинен глиом и други дифузни неоплазми на ствола се лекуват с лъчетерапия и противотуморна лекарствена терапия. В такива случаи не е необходима верификация. |
Пациентите с квадриплегичен пластинков глиом се подлагат на систематично магнитно-резонансно изследване и клинично наблюдение след отстраняване на церебралното хидроцеле. Ако неоплазмата показва признаци на растеж, тя се отстранява с допълнително облъчване. |
Когато се извършва частична резекция или биопсия на нискостепенен злокачествен глиом, пациентите с два или повече рискови фактора задължително се лекуват с лъчетерапия и/или химиотерапия. |
Тоталната резекция е задължителна при пациенти със субепендимален гигантоклетъчен астроцитом. |
Еверолимус се предписва за дифузен субепендимален гигантоклетъчен астроцитом. |
Пилоидният астроцитом трябва да се отстрани с магнитно-резонансна томография след интервенцията, за да се изясни качеството на радикалната резекция на туморната тъкан. |
При глиобластом, постоперативната терапия трябва да се комбинира (лъчетерапия + химиотерапия) с приложение на Темозоломид. |
При анапластичен астроцитом след операция е показана лъчетерапия с допълнителна лекарствена терапия. Използват се ломустин, темозоломид. |
Пациентите с анапластичен олигодендроглиом или олигоастроцитом получават едновременно лъчетерапия и химиотерапия (монотерапия с темозоломид или PCV) след операцията. |
Пациенти в напреднала възраст с обширен високозлокачествен глиом се облъчват в хипофракциониран режим или се провежда монотерапия с Темозоломид. |
В случай на рецидив на глиом, възможността за повторна операция и последващите тактики на лечение се обсъждат от консилиум от специалисти. Оптималният режим при рецидиви: повторна операция + системна химиотерапия + многократно лъчетерапия + палиативни мерки. При наличие на локализирани незначителни области на рецидивиращ туморен растеж може да се използва радиохирургия. |
Лекарствата по избор при рецидивиращ растеж на глиома са Темозоломид и Бевацизумаб. |
Рецидивът на силно злокачествени олигодендроглиоми и анапластични астроцитоми е показание за лечение с темозоломид. |
Плеоморфният ксантоастроцитом се отстранява без задължителна адювантна химиотерапия. |
Една от особеностите на глиомите е трудността при тяхното лечение и отстраняване. Хирургът се стреми да премахне тъканите на неоплазмата възможно най-пълно, за да постигне компенсация на състоянието. Много пациенти успяват да подобрят качеството на живот и да го удължат, но при силно злокачествени тумори прогнозата остава неблагоприятна: има повишена вероятност от повторен растеж на патологичния фокус.
Хранене при глиом на мозъка
Диета за пациенти със злокачествени тумори - важен момент, на който, за съжаление, много хора не обръщат особено внимание. Междувременно, благодарение на промените в диетата, е възможно да се забави развитието на глиома и да се засили и разклатеният имунитет.
Основни области на промяна в храненето:
- Нормализиране на метаболитните процеси, укрепване на имунната защита;
- Детоксикация на тялото;
- Оптимизация на енергийния потенциал;
- Осигуряване на нормалното функциониране на всички органи и системи на тялото през такъв труден за тях период.
Рационалното и балансирано хранене е необходимо както при пациенти с ранни стадии на нискокачествени злокачествени неоплазми, така и при пациенти с последен стадий на глиобластом. Внимателно подбраната диета допринася за подобряване на общото състояние, възстановяване на увредените тъкани, което е особено важно на фона на цитостатично и лъчетерапия. Балансът на хранителните компоненти и правилните метаболитни процеси предотвратяват образуването на инфекциозни огнища, блокират възпалителните реакции, предотвратяват изтощението на организма.
Следните храни и напитки се препоръчват за мозъчен глиом:
- Червени, жълти и оранжеви плодове и зеленчуци (домати, праскови, кайсии, моркови, цвекло, цитрусови плодове), съдържащи каротеноиди, които предпазват здравите клетки от негативните ефекти на лъчетерапията;
- Зеле (карфиол, броколи, брюкселско зеле), репички, горчица и други растителни продукти, които съдържат индол - активно вещество, което неутрализира неблагоприятните токсични и химични фактори;
- Зеленчуци (копър, магданоз, млади листа от глухарче и коприва, ревен, рукола, спанак), зелен грах и аспержи, аспержи и водорасли (морски водорасли, спирулина, хлорела);
- Зелен чай;
- Чесън, лук, ананас, които имат противотуморни и детоксикиращи свойства;
- Трици, зърнени храни, пълнозърнест хляб, покълнали кълнове от бобови растения, зърнени храни и семена;
- Тъмно грозде, малини, ягоди и ягоди, боровинки, къпини, нар, френско грозде, касис, офика, боровинки, морски зърнастец, череши и други горски плодове, които съдържат естествени антиоксиданти, намаляващи негативните ефекти на свободните радикали, вирусите и канцерогените;
- Нискомаслени млечни продукти.
Не бива да натоварвате храносмилателната система и цялото тяло с тежки и мазни храни. Полезно е да използвате прясно изцедени домашни сокове, смутита, хапки. Към ястията трябва да се добавят източници на омега-3 мастни киселини, като рибено масло, ленено масло или ленени семена.
По-добре е да избягвате захарта и сладкишите напълно. Но лъжица мед с чаша вода няма да навреди: пчелните продукти имат изразен противовъзпалителен, антиоксидантен и противотуморен ефект. Единственото противопоказание за употребата на мед е алергията към продукта.
От диетата трябва да се изключат:
- Месо, свинска мас, карантии;
- Масло, мазни млечни продукти;
- Пушено месо, колбаси, консервирано месо и риба;
- Алкохол под каквато и да е форма;
- Сладкиши, тестени изделия, торти и сладкиши, бонбони и шоколади;
- Удобни храни, бързо хранене, закуски;
- Пържени храни.
Трябва да консумирате достатъчно зеленчуци, зеленина, плодове и чиста питейна вода ежедневно.
По време на химиотерапията и известно време след нея трябва да пиете домашно приготвени зеленчукови и плодови сокове, да ядете домашно приготвена нискомаслена извара, мляко и сирене. Важно е да пиете много течности, да си миете зъбите и да изплаквате устата често (около 4 пъти на ден).
Оптимални хранения за пациенти с мозъчен глиом:
- Зеленчукови гювечи;
- Гарнитури и супи от зърнени храни (за предпочитане елда, овесени ядки, ориз, кускус, булгур);
- Чийзкейкове на пара, пудинги, гювечи;
- Задушени и печени зеленчуци;
- Яхнии, зеленчукови супи, първи и втори ястия от бобови растения (включително соя), пастети и суфлета;
- Смутита, зелен чай, компоти и хапки.
Предотвратяване
Ако човек води здравословен начин на живот и сред неговите роднини не е имало случаи на ракова патология, той има всички шансове да не се разболее от глиом на мозъка. Няма специфична превенция на такива тумори, така че основните превантивни точки се считат за правилно хранене, физическа активност, избягване на лоши навици, липса на професионални и битови опасности.
Специалистите дават редица прости, но ефективни препоръки:
- Пийте повече чиста вода, избягвайте подсладени газирани напитки, пакетирани сокове, енергийни напитки и алкохол.
- Избягвайте професионални и битови опасности: по-малко контакт с химикали, корозивни разтвори и течности.
- Опитайте се да приготвяте храна чрез варене, задушаване, печене, но не и пържене. Давайте предпочитание на здравословни, качествени домашно приготвени храни.
- Голяма част от диетата ви трябва да се състои от растителни храни, включително зелени, независимо от времето на годината.
- Друг негативен фактор е наднорменото тегло, от което трябва да се отървем. Контролът на теглото е много важен за здравето на цялото тяло.
- Растителните масла винаги трябва да се предпочитат пред маслото и свинската мас.
- Ако е възможно, е желателно да се даде предимство на екологично чисти продукти, месо без хормони, зеленчуци и плодове без нитрати и пестициди. По-добре е да се избягва изцяло червеното месо.
- Не приемайте мултивитаминни препарати без показания и в големи количества. Не приемайте никакви лекарства без лекарско предписание: самолечението често е много, много опасно.
- Ако се появят подозрителни симптоми, е необходимо да посетите лекар, без да чакате влошаване на ситуацията, развитие на нежелани реакции и усложнения.
- Сладките храни и храните с висок гликемичен индекс са нежелан компонент от диетата.
- Колкото по-рано човек отиде на лекар, толкова по-големи са шансовете му за излекуване (и това важи за почти всяко заболяване, включително глиом на мозъка).
За да предотвратите образуването на онкопатология, е необходимо достатъчно време за сън и почивка, избягвайте прекомерната консумация на алкохолни напитки, дайте предимство на висококачествена натурална храна, намалете използването на джаджи (по-специално мобилни телефони).
Туморните заболявания често се срещат при възрастни и стари хора. Ето защо е важно да следите собственото си здраве от ранна възраст и да не провокирате патологични процеси чрез нездравословен начин на живот и вредни навици.
Точните коренни причини за онкологията все още не са изяснени. Разбира се, определена роля играят неблагоприятните професионални и екологични условия, излагането на йонизиращо и електромагнитно лъчение, хормоналните промени. Не стойте дълго и редовно на слънце, не допускайте резки промени в температурата на околната среда, не прегрявайте във ваната или сауната, не приемайте често горещи вани или душове.
Друг въпрос: как да се предотврати рецидив на мозъчен глиом след успешното му лечение? Рецидивът на растежа на неоплазмата е сложно и, за съжаление, често срещано усложнение, което е трудно да се предвиди предварително. На пациентите може да се препоръча да се подлагат на редовни профилактични прегледи и контролни прегледи, да посещават онколог и лекуващ лекар поне два пъти годишно, да водят здравословен начин на живот, да се хранят със здравословна и натурална храна, да практикуват умерена физическа активност. Друго условие е любовта към живота, здравословният оптимизъм, позитивното отношение към успеха при всякакви обстоятелства. Това включва и приятелска атмосфера в семейството и на работното място, търпение и безусловна подкрепа от близки хора.
Прогноза
Състоянието на мозъка и характеристиките на глиома към момента на откриването му влияят върху процента на преживяемост, както и приложеното лечение. Задоволителното общо здравословно състояние на пациента и неговата възраст подобряват прогнозата (прогнозата е по-оптимистична при млади пациенти). Важен показател е хистологичната картина на неоплазмата. По този начин, нискостепенните глиоми имат по-добра прогноза от анапластичните глиоми и, още повече, глиобластомите (най-неблагоприятните туморни процеси). Астроцитомите имат по-лоша прогноза от олигодендроглиомите.
Злокачествените астроцитоми реагират слабо на терапия и имат относително нисък процент на преживяемост от шест до пет години. В същото време, продължителността на живота при нискостепенните глиоми се оценява на 1-10 години.
Злокачествените астроцитоми са по същество нелечими. Насоката на лечение обикновено включва намаляване на неврологичните прояви (включително когнитивна дисфункция) и увеличаване на продължителността на живота, като същевременно се поддържа възможно най-високо качество на живот. Симптоматичната терапия се привлича на фона на рехабилитационни мерки. Работата на психолог също е важна.
През последното десетилетие учените постигнаха известен напредък в разбирането на природата на мозъчните тумори и как да ги лекуват. Трябва да се направи много повече, за да се оптимизира прогнозата на заболяването. Основната задача на специалистите днес е следната: мозъчният глиом трябва да има няколко схеми за ефективно елиминиране на проблема едновременно, както в ранните, така и в последващите етапи на развитие.

