Нови публикации
Изследване на механизма на лекарствените обриви върху кожата
Последно прегледани: 02.07.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
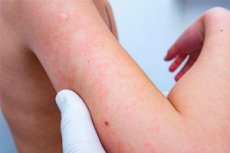
Въпреки че лекарствата често помагат на пациентите да излекуват или облекчат състоянието си, милиони хора по света страдат от непредсказуеми токсични реакции към лекарства всяка година. По-специално, лекарствените обриви, които включват симптоми като зачервяване, мехури и сърбеж на кожата, са доста често срещани.
Тежките лекарствени реакции могат да бъдат животозастрашаващи и да имат дълготрайни последици. Следователно, разбирането как и защо възникват лекарствени реакции е важна област на изследване в медицинската наука.
За тази цел, предишни проучвания са идентифицирали специфични варианти на определени гени като потенциални причинители на лекарствени обриви. Учените смятат, че гени, кодиращи човешки левкоцитен антиген (HLA), протеин, експресиран на повърхността на белите кръвни клетки, който играе важна роля в имунната система, участват в развитието на лекарствени обриви. Съвременните теории обаче не могат да обяснят защо свързаните с HLA лекарствени обриви обикновено се появяват по кожата, а не в множество органи в тялото.
За да се запълни тази празнина в знанията, изследователски екип, включващ преподавателите Шигеки Аоки, Кусей Ито и Акира Казаока от Висшето училище по медицински и фармацевтични науки към Университета Чиба, проведе задълбочено проучване на връзката между HLA и лекарствените обриви. Техните открития бяха публикувани в PNAS Nexus.
Първоначално изследователите провели серия от експерименти върху миши кератиноцити, които са основният тип клетки, открити в кожата. Тези кератиноцити били модифицирани, за да експресират специфичен вариант на HLA гена, наречен HLA-B57:01, който се свързва специфично с антивирусното лекарство абакавир. След това те потвърдили тези резултати при генетично модифицирани мишки, експресиращи HLA-B 57:01, които били изложени на абакавир.
Изследователите установили, че кератиноцитите, експресиращи HLA-B*57:01 и изложени на абакавир, показват стрес реакции на ендоплазмения ретикулум (ЕР), като незабавно освобождаване на калций в цитозола и повишена експресия на топлинен шоков протеин 70 (HSP70). Те също така наблюдавали повишено производство на цитокини и миграция на имунните клетки. Излагането на абакавир е причинило неправилно сгъване на HLA в ЕР, което е довело до стрес в ЕР.
Освен това, изследователите открили, че стресът в ендоплазмения ретикулум може да бъде намален с помощта на 4-фенилбутират (4-PB). Чрез елиминирането на този стрес, те са успели да потиснат появата на тежки симптоми на лекарствен обрив. Това ново знание може да осигури основата за иновативни възможности за лечение на лекарствени обриви.
Но как тази нова информация контрастира с това, което вече беше известно за HLA?
„HLA молекулите са неразделна част от нашата имунна система, като обикновено представят чужди антигени на белите кръвни клетки, които оценяват тези антигени като свои или не-свои. В тази установена роля HLA обикновено играе второстепенна роля“, обяснява д-р Аоки.
„Нашето проучване обаче подчертава нова функция на HLA молекулата в кожните клетки. Установихме, че специфичен HLA генотип в кератиноцитите може да разпознае определени лекарства като чужди, предизвиквайки стресова реакция на ендоплазмения ретикулум.“
Взети заедно, резултатите от това проучване разкриват нова роля на HLA протеините в откриването и реагирането на потенциални заплахи в кожните клетки. Следователно техните функции могат да се простират далеч отвъд простото представяне на антигени на имунната система. Освен това, като се има предвид, че HLA вариантът на индивида може да бъде определен чрез генетично тестване, това проучване може да помогне за разработването на превантивни мерки и диагностични методи срещу тежки нежелани лекарствени реакции.
Според д-р Аоки това е в съответствие със съвременните тенденции и насоки в медицинската наука. „След 10 години очакваме да навлезем в ерата на „всеобхватния геном“, където персонализираната медицина, базирана на индивидуалните геноми, ще се превърне в стандартна практика“, коментира той.
„Въз основа на резултатите от това проучване, ние вярваме, че цялостното разбиране на механизма, който е в основата на HLA-зависимите нежелани лекарствени реакции, ще позволи безопасна медицинска помощ, позволявайки на пациентите да избегнат ненужно страдание, дължащо се на странични ефекти.“
Като цяло, бъдещите изследвания в тази област могат да сведат до минимум появата на лекарствени обриви и да предпазят хората от потенциално фатални нежелани лекарствени реакции.
