Ново устройство подобрява генерирането на стволови клетки за терапия на Алцхаймер
Последно прегледани: 14.06.2024

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.

Изследователи в Швеция казват, че са усъвършенствали техника за превръщане на нормални кожни клетки в неврални стволови клетки, което според тях се доближава до достъпни персонализирани клетъчни терапии за лечение на болестта на Алцхаймер и Паркинсон.
Използвайки специално проектирано микрофлуидно устройство, изследователският екип разработи безпрецедентен и ускорен подход за препрограмиране на човешки кожни клетки в индуцирани плурипотентни стволови клетки (iPSC) и след това да ги развие в нервни стволови клетки.
Първият автор на изследването, Saumey Jain, казва, че платформата може да подобри и намали цената на клетъчната терапия, като направи клетките по-лесни за съвместимост и приемане от тялото на пациента. Изследването е публикувано в Advanced Science от учени от Кралския технологичен институт KTH.
Анна Херланд, старши автор на изследването, каза, че проучването демонстрира първото използване на микрофлуиди за насочване на iPSC да станат нервни стволови клетки.
Неврални стволови клетки, диференцирани с помощта на микрофлуидна платформа. Снимка: KTH Royal Institute of Technology
Трансформацията на обикновени клетки в неврални стволови клетки всъщност е процес в две стъпки. Клетките първо са изложени на биохимични сигнали, които ги индуцират в плурипотентни стволови клетки (iPSCs), които могат да генерират различни видове клетки.
След това те се прехвърлят в култура, която имитира сигналите и процесите на развитие, участващи във формирането на нервната система. Този етап, наречен неврална диференциация, пренасочва клетките към пътя на невралните стволови клетки.
През последните десет години лабораторните среди за такава работа постепенно се изместиха от традиционните плочи към микрофлуидни устройства. Herland казва, че новата платформа представлява подобрение в микрофлуидиката и за двете стъпки: генериране на iPSC и диференциация на нервни стволови клетки.
Използвайки клетки от биопсии на човешка кожа, изследователите установиха, че микрофлуидната платформа дава възможност на клетките да се ангажират с невронна съдба на по-ранен етап от тези, диференцирани в конвенционалните плаки.
„Ние документираме, че ограничената среда на микрофлуидната платформа засилва ангажимента за генериране на нервни стволови клетки“, казва Херланд.
Най-близкият изглед на микрофлуиден чип, използван за индукция на стволови клетки. Снимка: KTH Royal Institute of Technology
Джейн казва, че микрофлуидният чип може лесно да бъде произведен с помощта на полидиметилсилоксан (PDMS) и неговият микроскопичен размер предлага значителни икономии на реагенти и клетъчен материал.
Платформата може лесно да се модифицира, за да се адаптира към диференциация в други типове клетки, добавя той. Може да се автоматизира, осигурявайки затворена система, която гарантира последователност и надеждност при производството на силно еднородни популации от клетки.
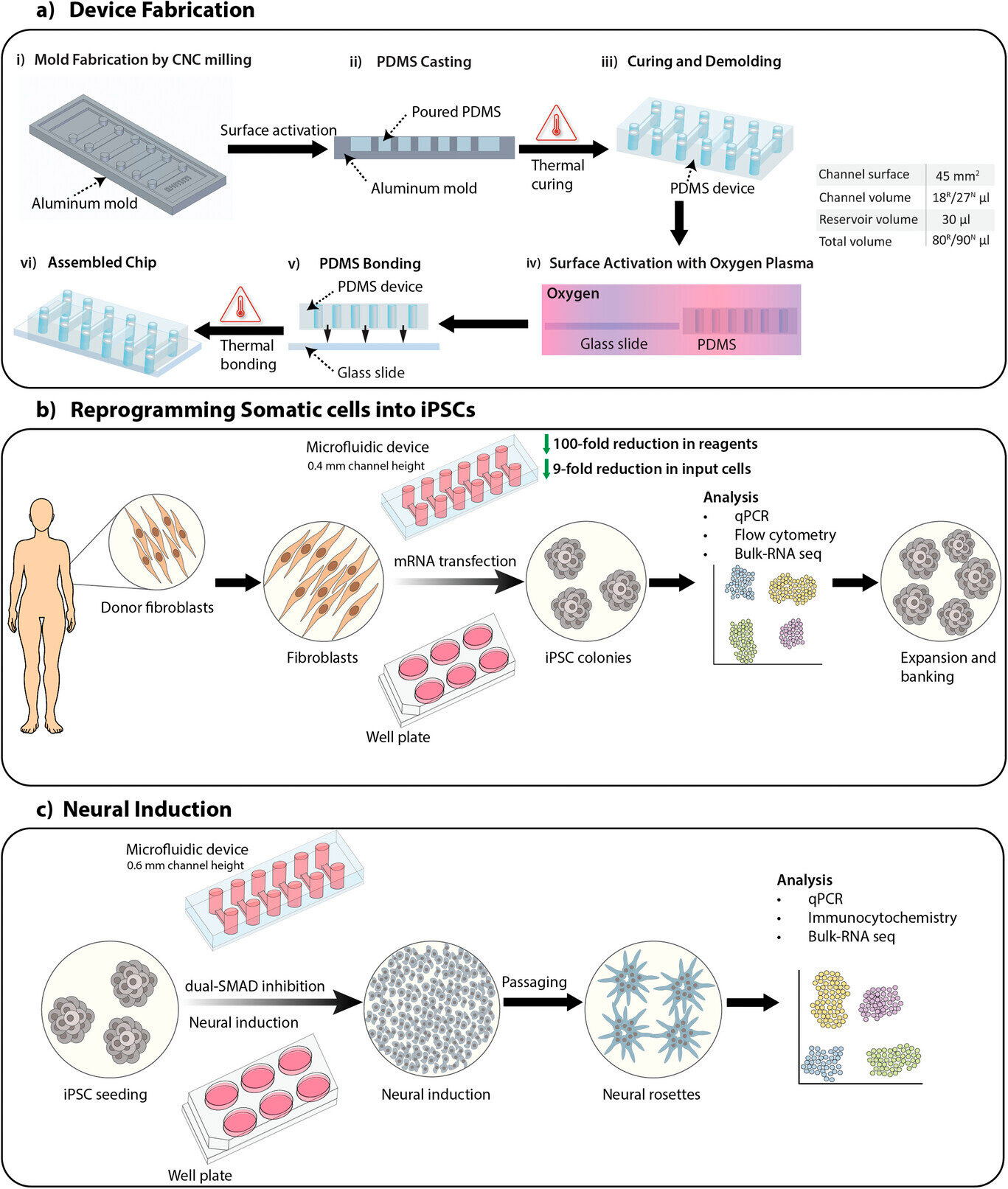
Преглед на изследванията, включително производство на устройства, препрограмиране на соматични клетки в индуцирани плурипотентни стволови клетки (iPSCs) и неврална индукция на iPSCs с помощта на протокола за двойно SMAD инхибиране за генериране на невронни стволови клетки.
а) Процес на производство на микрофлуидно устройство с канали с височина 0, 4 и 0, 6 mm съответно за препрограмиране на соматични клетки (R) и невронна индукция (N). Обемите на каналите и общият обем са посочени в таблицата.
б) Преглед на процеса на препрограмиране на соматични клетки в iPSC върху микрофлуидни устройства и плаки, използвайки трансфекция на иРНК.
в) Преглед на процеса на неврална индукция на iPSCs в неврални стволови клетки върху микрофлуидни устройства и плаки, използвайки протокола за двойно инхибиране SMAD.
Източник: Advanced Science (2024). DOI: 10.1002/advs.202401859
„Това е стъпка към това да направим персонализирани клетъчни терапии за болестите на Алцхаймер и Паркинсон достъпни“, добавя Джейн.
Учени от Karolinska Institutet и университета в Лунд също участваха в проучването, като си сътрудничиха в консорциума IndiCell.
