Нови публикации
FDA одобрява нова терапия за пациенти с глиом за първи път от десетилетия насам
Последно прегледани: 02.07.2025

Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
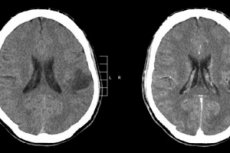
Ворасидениб е одобрен от Американската агенция по храните и лекарствата (FDA) за пациенти с глиоми степен 2 с IDH1 или IDH2 мутации.
Въз основа на данни от клиничното проучване INDIGO, глобално, двойносляпо, рандомизирано клинично проучване фаза III, ворасидениб е увеличил преживяемостта без прогресия повече от два пъти и е забавил необходимостта от лечение с лъчетерапия и химиотерапия при пациенти с глиом степен 2 с IDH мутация след операция за резекция на тумора. INDIGO е първото клинично проучване фаза III на таргетна терапия за глиом с IDH мутация.
„Проучването INDIGO показва, че инхибиторите на IDH могат да работят при нискостепенни глиоми с IDH мутация“, казва д-р Патрик Уен, директор на Центъра за невроонкология в Онкологичния институт „Дана-Фарбър“ и един от тримата председатели на проучването. „Последното лекарство, одобрено за нискостепенни глиоми, е одобрено през 1999 г., така че това би било първото ново лекарство от дълго време.“
Глиомите от втора степен са нелечими мозъчни тумори. IDH мутации се откриват в по-голямата част от нискостепенните глиоми.
Ключово предимство на терапията с воразидениб е, че тя може да забави необходимостта от лъчетерапия и химиотерапия. Сегашното лечение включва хирургическа намеса, последвана от лъчетерапия и химиотерапия. Лъчетерапията и химиотерапията са ефективни лечения, но след много години лечение пациентите започват да изпитват признаци на когнитивна дисфункция, които обикновено се наблюдават при много по-възрастни хора.
„Тези пациенти често са млади, на 30 или 40 години. Но 10 до 20 години по-късно, дори и да се справят добре по отношение на тумора си, те често показват признаци на деменция след лъчетерапия и химиотерапия“, казва Уен. „Ако това лекарство може да забави началото на тези лечения, то може да забави когнитивната дисфункция при пациентите и да запази качеството им на живот.“
Проучването INDIGO включва 331 пациенти с глиоми степен 2 с IDH-мутация, които са претърпели операция за отстраняване на тумора. Пациентите, включени в проучването, не са се нуждаели от незабавна лъчетерапия или химиотерапия и са били в период на проследяване. През този период те са били рандомизирани да получават ворасидениб или плацебо.
Пациентите, приемащи ворасидениб, са имали медиана на преживяемост без прогресия от 27,7 месеца, в сравнение с 11,1 месеца за пациентите, приемащи плацебо. Времето до следващото лечение за пациентите, приемащи плацебо, е било 17,8 месеца.
При пациенти, лекувани с ворасидениб, медианата не е определена към момента на последния анализ, тъй като само 11,3% от тези пациенти са преминали към следващото лечение досега. Лекарството също така има управляем профил на безопасност.
„Проучването не установи разлика в качеството на живот в сравнение с плацебо“, казва Уен. „Поносимостта е важна, защото това е лекарство, което очакваме хората да приемат в продължение на много години.“
Одобрението открива няколко нови възможности за пациентите. Например, Van има текущо проучване, разглеждащо ворасидениб в комбинация с имунотерапия, а също така са планирани проучвания, комбиниращи ворасидениб със стандартна лъчетерапия и химиотерапия.
